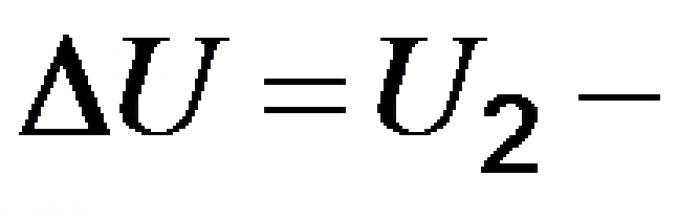Теоретические сведения
Химический процесс можно рассматривать как первую ступень при восхождении от химических объектов – электрон, протон, атом – к живой системе.
Учение о химических процессах – это область науки, в которой существует наиболее глубокое взаимопроникновение физики, химии, биологии. В основе этого учения находятся химическая термодинамика и кинетика.
Способность вещества подвергаться химическим превращениям определяется их реакционной способностью, т.е. природой реагирующих веществ – составом, строением, характером химической связи; энергетическими факторами, определяющими возможность протекания процесса и кинетическими факторами, определяющими скорость его протекания.
Почти все химические процессы сопровождаются выделением или поглощением энергии, чаще всего в форме теплоты и работы.
Теплота – количественная мера беспорядочного хаотичного движения частиц, образующих данную систему.
Работа – количественная мера упорядоченного движения частиц в направленном силовом поле.
Раздел химии, изучающей переходы энергии из одой формы в другую при химических реакциях и устанавливающая направление и пределы их самопроизвольного протекания при заданных условиях, называется химической термодинамикой .
Объектом изучения химической термодинамики является химическая система.
Система – это изучаемое тело или группа тел, которые взаимодействуют между собой и мысленно или реально отделены от окружающей среды границами, проводящими или не проводящими тепло.
В зависимости от характера взаимодействия системы с окружающей средой различают открытые, закрытые и изолированные системы.
Открытые системы могут обмениваться с окружающей средой энергией и веществом. Например, водный раствор хлорида натрия, находящийся в открытом сосуде. При испарении воды из раствора и при теплообмене будут меняться масса системы и ее температура, а, следовательно, и энергия.
Закрытые системы не обмениваются с окружающей средой веществом. Например, раствор хлорида натрия в закрытом сосуде. Если раствор и окружающая среда имеют разную температуру, то будет происходить нагревание или охлаждение раствора, а, следовательно, будет меняться его энергия.
Изолированные системы не могут обмениваться со средой ни веществом, ни энергией. Изолированная система – это идеализация. В природе таких систем нет. Но, несмотря на невозможность практического воплощения, изолированные системы позволяют определять максимальные теоретические разности энергий между системой и ее окружением.
Состояние системы определяется совокупностью свойств и характеризуется термодинамическими параметрами : температурой (), давлением (), объемом (), плотностью (), количеством вещества (), совершаемой работой (), теплотой (). Изменение хотя бы одного термодинамического параметра приводит к изменению состояния системы в целом. Если все параметры постоянны во времени и пространстве, то такое состояние системы называется равновесным .
В термодинамики свойства системы рассматриваются в ее равновесных состояниях: начальных и конечных, вне зависимости от пути перехода системы из одного состояния в другое. Переход системы из одного состояния в другое при , = const называется изобарно-изотермическим, при , = const – изохорно-изотермическим.
Важнейшими задачами химической термодинамики является выяснение возможности или невозможности самопроизвольного протекания процесса той или иной химической реакции при заданных условиях и в заданном направлении; установление значения термодинамических параметров, при которых достигается максимальный выход процесса; определение характеристик энергетического изменения, происходящего в системе. Находят это с помощью термодинамических функций ().
Функция состояния характеризует внутреннюю энергию системы – сумму потенциальной энергии взаимодействия всех частиц тела между собой и кинетической энергии их движения. Она зависит от состояния вещества – вида, массы, агрегатного состояния. Абсолютную величину внутренней энергии измерить невозможно. Для изучения химических процессов важно знать только изменение внутренней энергии при переходе системы из одного состояния в другое.
 (27)
(27)
При этом  внутренняя энергия системы убывает, при
внутренняя энергия системы убывает, при  - возрастает. Все изменения внутренней энергии происходят за счет хаотического столкновения молекул (мерой передаваемой таким способом энергии является теплота) и перемещения масс, состоящих из большого числа частиц, под действием каких-либо сил (мерой передаваемой таким способом энергии является работа). Таким образом передача внутренней энергии может осуществляться частично в виде теплоты и частично в виде работы:
- возрастает. Все изменения внутренней энергии происходят за счет хаотического столкновения молекул (мерой передаваемой таким способом энергии является теплота) и перемещения масс, состоящих из большого числа частиц, под действием каких-либо сил (мерой передаваемой таким способом энергии является работа). Таким образом передача внутренней энергии может осуществляться частично в виде теплоты и частично в виде работы:
 (28)
(28)
Приведенное уравнение представляет собой математическое выражение I закона термодинамики : если к системе подвести тепло, то подведенное тепло тратится на увеличение внутренней энергии системы и на совершение ей работы.
В изохорно-изотермическом процессе вся теплота, подведенная к системе, тратится на изменение внутренней энергии:
 (29)
(29)
В изобарно-изотермическом процессе единственным видом работы, совершаемой системой, является работа расширения:
 (30)
(30)
где - давление в системе, - изменение объема
Тогда математическое выражение I закона термодинамики принимает вид:  (31)
(31)
Обозначив  , получаем
, получаем 
Функция состояния системы Н – энтальпия – это общий запас энергии системы, т.е. это энергосодержание системы. Энтальпия системы больше внутренней энергии на величину работы.
Для характеристики энергетических проявлений в ходе реакции введено понятие тепловой эффект.
Тепловой эффект
– это количество теплоты, которое выделяется или поглощается при необратимом протекании реакции, когда единственной работой будет работа расширения. При этом температуры исходных веществ и продуктов реакции должны быть одинаковыми. Тепловой эффект эндотермической реакции
(протекает с поглощением тепла) будет положительным:  ,
,  . Тепловой эффект экзотермической реакции
(протекает с выделением тепла) будет отрицательным:
. Тепловой эффект экзотермической реакции
(протекает с выделением тепла) будет отрицательным:  ,
,  .
.
Раздел химии, посвященный изучению тепловых эффектов химических реакций, называется термохимией .
Всякая химическая реакция сопровождается изменениями запаса энергии реагирующих веществ. Чем больше энергии выделилось при образовании какого-либо химического соединения, тем это соединение устойчивее, и, наоборот, вещество, полученное в результате эндотермической реакции, неустойчивое.
В химических уравнениях, в которых указана теплота реакции, называются термохимическими. Они составляются на основе законов сохранения массы и энергии.
Для сравнения тепловых эффектов различных процессов стандартизуют условия их протекания. Стандартные условия - Т 0 = 298 К, р 0 = 101,313 кПа, n – 1 моль чистого вещества, изменение энтальпии ( ) относят к единице количества вещества, кДж/моль.
Все стандартные термодинамические функции – это табличные величины
, которые зависят от агрегатного состояния вещества.
) относят к единице количества вещества, кДж/моль.
Все стандартные термодинамические функции – это табличные величины
, которые зависят от агрегатного состояния вещества.
Из I закона термодинамики следуют количественные законы термохимии.
Закон Лавуазье-Лапласа (1780 – 1784) – для каждого химического соединения теплота разложения равна теплоте его образования, но имеет противоположный знак.
Закон Г.И. Гесса (1840) – тепловой эффект химической реакции зависит от природы и физического состояния исходных веществ и конечных продуктов, но не зависит от характера и пути протекания реакции, т.е. от последовательности отдельных промежуточных стадий. Данный закон – теоретическая основа термохимии. Из него вытекает ряд следствий:
В термохимических расчетах теплота образования (энтальпия) простых веществ в стандартных условиях принимается равной нулю.
 (простого вещества
) = 0
(простого вещества
) = 0
Количество энергии, которое выделяется или поглощается при образовании 1 моль сложного вещества из простых в стандартных условиях, называется стандартной энтальпией образования ( , кДж/моль).
, кДж/моль).
Количество энергии, которое выделяется или поглощается 1 моль органического вещества разлагающегося до углекислого газа и воды в стандартных условиях, называется стандартной энтальпией сгорания ( , кДж/моль).
, кДж/моль).
Тепловой эффект химической реакции равен разности между суммой теплот образования продуктов реакции и суммой теплот образования исходных веществ с учетом стехиометрических коэффициентов:
где - тепловой эффект химической реакции в стандартных условиях;  - сумма стандартных теплот образования продуктов реакции;
- сумма стандартных теплот образования продуктов реакции;  - сумма стандартных теплот образования исходных веществ;
- сумма стандартных теплот образования исходных веществ;  ,
,  - стехиометрические коэффициенты соответственно продуктов реакции и исходных веществ.
- стехиометрические коэффициенты соответственно продуктов реакции и исходных веществ.
Закон Гесса позволяет рассчитать тепловые эффекты различных реакций. Но знак и величина теплового эффекта не позволяет судить о способности процессов к самопроизвольному протеканию и не содержит информации о направлении и полноте протекания процессов.
Самопроизвольные процессы (естественные или положительные) – протекают в системе без вмешательства со стороны внешней среды и сопровождаются уменьшением внутренней энергии системы и передачей энергии в окружающую среду в форме теплоты и работы. Эндотермические самопроизвольные процессы не противоречат этому определению, так как они могут протекать в неизолированной системе и производить работу за счет теплоты окружающей среды.
Процессы, которые сами собой (без внешнего воздействия) совершаться не могут, называются несамопроизвольными , неестественными или отрицательными. Такие процессы осуществляются путем передачи системе энергии из внешней среды в форме теплоты или работы.
Согласно II закону термодинамики самопроизвольные процессы идут в сторону уменьшения запаса внутренней энергии или энтальпии системы. Однако известны такие процессы, которые протекают самопроизвольно без изменения внутренней энергии системы. Движущей силой таких процессов является энтропия системы.
Энтропия
(связанная энергия)(
S)
– это мера необратимости процесса, мера перехода энергии в такую форму, из которой она не может самостоятельно в другую энергию. Энтропия характеризует беспорядок в системе, чем выше беспорядок, тем выше энтропия. Она возрастает с увеличением движения частиц. В изолированных от внешней среды системах процессы протекают самопроизвольно в направлении увеличения энтропии (). Процессы, для которых энтропия уменьшается ( ) неосуществимы в изолированных системах. Если процесс возможен в прямом и обратном направлениях, то в изолированной системе он будет протекать в направлении возрастания энтропии. Протекание самопроизвольного процесса в изолированной системе завершается состоянием равновесия. Следовательно, в состоянии равновесия энтропия системы максимальна
.
) неосуществимы в изолированных системах. Если процесс возможен в прямом и обратном направлениях, то в изолированной системе он будет протекать в направлении возрастания энтропии. Протекание самопроизвольного процесса в изолированной системе завершается состоянием равновесия. Следовательно, в состоянии равновесия энтропия системы максимальна
.
Больцман вывел уравнение, согласно которому
(34) где - постоянная Больцмана, W – вероятность состояния, определяет число микросостояний, соответствующих данному микросостоянию.
Это соотношение показывает, что энтропию можно рассматривать как меру молекулярного беспорядка системы.
Согласно II закону термодинамики для изотермического процесса изменение энтропии равно:
 ; [Дж/(моль·К] (35)
; [Дж/(моль·К] (35)
Энтропия простых веществ не равна нулю. В отличие от энтальпии, можно измерить абсолютное значение энтропии. «При абсолютном нуле энтропия идеального кристалла равна нулю» - этот постулат М. Планка (1911 г) называют III законом термодинамики.
Изменение энтропии химического процесса определяется балансовым уравнением:
Любая система характеризуется порядком () и беспорядком (). Их соотношение определяет направление протекания реакции.
Таким образом, при самопроизвольном движении системы к устойчивому состоянию проявляются две тенденции: уменьшение энтальпии  и возрастание энтропии . Суммарный эффект двух тенденций при постоянной температуре и давлении отражает изобарно-изотермический потенциал или энергия Гиббса ()
.
и возрастание энтропии . Суммарный эффект двух тенденций при постоянной температуре и давлении отражает изобарно-изотермический потенциал или энергия Гиббса ()
.
Функция состояния
характеризует общую движущую силу процесса, максимально возможную полезную работу («свободная энергия»), совершаемую системой ;  - часть энергии, которая не может быть превращена в полезную работу («связанная энергия»).
- часть энергии, которая не может быть превращена в полезную работу («связанная энергия»).
Химические реакции протекают в открытом сосуде с изменением объема, поэтому возможность (самопроизвольность) и направление процесса характеризует функция , определяемая по балансовому уравнению при стандартных условиях:
;  (38)
(38)
Самопроизвольному протеканию процесса отвечает уменьшение энергии Гиббса,  . Чем больше уменьшается , тем более необратимо протекает процесс в сторону образования конечных продуктов реакции. Увеличение изобарного потенциала
. Чем больше уменьшается , тем более необратимо протекает процесс в сторону образования конечных продуктов реакции. Увеличение изобарного потенциала  является признаком неосуществимости процесса в данных условиях. Значение
является признаком неосуществимости процесса в данных условиях. Значение  характеризует состояние равновесия, т.е. состояние, в котором система не производит полезной работы.
характеризует состояние равновесия, т.е. состояние, в котором система не производит полезной работы.
Анализ величин и в уравнении Гиббса показал, что возможность обратимого протекания процесса обусловлена одинаковыми знаками и . При определенной температуре величины и  становятся равными. Поэтому из уравнения Гиббса можно определить «равновесную» температуру или температуру начала процесса ():
становятся равными. Поэтому из уравнения Гиббса можно определить «равновесную» температуру или температуру начала процесса ():
 ; = 0
;
; = 0
;  ;
;  (39)
(39)
Таким образом, самопроизвольно протекают реакции, в которых изменение свободной энергии отрицательно. Реакции, в которых  , протекают лишь при условии, что над системой будет совершена работа внешними силами или системе будет передана энергия извне. Условия самопроизвольного протекания процесса показаны на рис. 3.
, протекают лишь при условии, что над системой будет совершена работа внешними силами или системе будет передана энергия извне. Условия самопроизвольного протекания процесса показаны на рис. 3.
Химические реакции, Химические реакции,
протекающие самопроизвольно протекающие не самопроизвольно


экзотермические реакции, экзотермические реакции,
сопровождающиеся сопровождающиеся
возрастанием энтропии уменьшением энтропии
при любых температурах при высоких температурах
эндотермические реакции
сопровождающиеся
возрастанием энтропии
при низких температурах
Рис. 3. Условия самопроизвольного протекания процесса.
3.2. Контрольные вопросы и задания
1. Что называется системой? Какими параметрами характеризуется система?
2. Охарактеризуйте внутреннюю энергию системы, понятие об изохорных и изобарных процессах.
3. Что называется энтальпией?
4. Охарактеризуйте энтальпию образования соединений, стандартные энтальпии сгорания и образования веществ.
5. Закон Гесса и его следствия, его применение в термохимических расчетах.
6. Определение теплот (энтальпий) нейтрализации, растворения, гидратации.
7. Энтропия. Уравнение Больцмана. Как изменяется энтропия с изменением температуры?
8. Энергия Гиббса. Критерии самопроизвольного протекания процесса.
9. Пользуясь справочными данными приложения 3, вычислите изменение стандартной энтальпии реакции ():
10. Пользуясь справочными данными приложения 3, вычислите изменение стандартной энтропии реакции ( ):
):
11. Вычислить реакции при 846 0 С, если = 230 кДж,  = 593 Дж/К.
= 593 Дж/К.
Примеры решения задач
Пример 1. Реакция горения этилового спирта выражается термохимическим уравнением С 2 Н 5 ОН (Ж) + 3О 2(Г) = 2СО 2(Г) + 3Н 2 О (Ж) . Вычислите тепловой эффект реакции, если известно, что молярная теплота парообразования С 2 Н 5 ОН (Ж) равна +42,36 кДж, а теплоты образования С 2 Н 5 ОН (Г) = -235,31 кДж, СО 2(Г) = -393,51 кДж, Н 2 О (Ж) = -285,84 кДж.
Решение. Для определения ΔΗ реакции необходимо знать теплоту образования С 2 Н 5 ОН (Ж) . Последнюю находим из данных:
С 2 Н 5 ОН (Ж) = С 2 Н 5 ОН (Г) ; ΔΗ = +42,36 кДж
42,36 = -235,31 – ΔΗ(С 2 Н 5 ОН (Ж))
ΔΗ(С 2 Н 5 ОН (Ж)) = -235,31-42,36 = -277,67 кДж
Вычисляем ΔΗ реакции, применяя следствия из закона Гесса:
ΔΗ Х.Р. = 2(-393,51) + 3(-285,84) + 277,67 = -1366,87 кДж.
Тепловой эффект реакции 1366,87 кДж.
а) Fe 2 O 3(К) + 3H 2(Г) = 2Fe (К) + 3H 2 O (Г)
б) Fe 2 O 3(К) + 3СО (Г) = 2Fe (К) + 3СО 2(Г)
В каком случае на этот процесс потребуется больше затратить энергии?
Решение. Для расчета ΔΗ ХР воспользуемся формулой следствия из закона Гесса и стандартными энтальпиями образования каждого вещества [Приложение 3]:
а) ΔΗ ХР = 2ΔΗ(Fe) + 3ΔΗ(H 2 O) – (ΔΗ(Fe 2 O 3) + 3ΔΗ(H 2)) = 2(0) + 3(-241,8) – ((-822,2) + 3(0)) = -725,4 + 822,2 = 96,8 кДж.
б) ΔΗ ХР = 2ΔΗ(Fe) + 3ΔΗ(СO 2) – (ΔΗ(Fe 2 O 3) + 3ΔΗ(СО)) = 2(0) + 3(-393,5) – ((-822,2) + 3(-110,5)) = -1180,5 + 822,2 + 331,5 = -26,5 кДж.
Согласно расчетам, процесс а) – восстановление оксида железа (III) водородом, требует больше затрат энергии, чем процесс б). В процессе б) реакция даже носит экзотермический характер (выделяется энергия в виде тепла).
Пример 3. Водяной газ представляет собой смесь равных объемов водорода и оксида углерода (II). Найдите количество теплоты, выделяющейся при сжигании 112 л водяного газа, (н.у.).
Решение. Составим термохимическое уравнение процесса:
Н 2(Г) + СО (Г) + О 2(Г) = Н 2 О (Г) + СО 2(Г) ΔΗ ХР = - Q.
Рассчитаем ΔΗ ХР, когда сгорает 2 моля водяного газа (1 моль Н 2 и й моль СО), т.е. 22,4 л/моль · 2 моль = 44,8 л. Расчет ведем по формуле следствия закона Гесса и стандартными энтальпиями образования каждого вещества [Доп. 3]:
ΔΗ ХР = ΔΗ(Н 2 О) + ΔΗ(СО 2) – (ΔΗ(Н 2) + ΔΗ(СО) + ΔΗ(О 2)) = -241,8 – 393,5 – (0 – 110,5 + 0) = - 635,3 + 110,5 = - 524,8 кДж
Составляем пропорцию:
Сгорает 44,8 л водяного газа – выделяется 524,8 кДж тепла
112 л - Х кДж
Х = 112 · 524,8 / 44,8 = 1312 кДж
При сжигании 112 л водяного газа выделяется 1312 кДж тепла.
Пример 4. Дайте термодинамическую характеристику процесса Ga + HCl) ↔ GaCl 3(т) + Н 2(г) по плану:
1. Запишите стехиометрическое уравнение.
2. Выпишите термодинамические функции участвующих веществ.
3. Рассчитайте изменение стандартной энтальпии химической реакции и постройте энтальпийную диаграмму.
4. Определите, является реакция экзо- или эндотермической; увеличивается или уменьшается температура в системе в результате протекания данной реакции.
5. Рассчитайте изменение стандартной энтропии реакции, объясните изменение энтропии в ходе реакции.
6. Рассчитайте стандартное изменение энергии Гиббса по балансовому уравнению и уравнению Гиббса. Дайте анализ полученным данным.
7. Сопоставьте знаки величин  . и
. и  Сделайте вывод об обратимости реакции.
Сделайте вывод об обратимости реакции.
8. Для обратимой реакции рассчитайте равновесную температуру согласно уравнению Гиббса допуская, что предельно допустимой температурой является 3000 К. Сделайте вывод: Тр – реализуема или не реализуема.
9. Рассчитайте величину  при трех значениях температур (500, 1000 и 1500 К). Постройте графическую зависимость
при трех значениях температур (500, 1000 и 1500 К). Постройте графическую зависимость  ..
..
10. Сделайте вывод о самопроизвольности протекания химической реакции. Определите условия, при которых реакция возможна
Решение.
1 Записываем стехиометрическое уравнение.
2. Выписываем стандартные термодинамические функции образования компонентов реакции (табл. 21) (термодинамические параметры веществ из [Приложение 3]).
Введение в физическую и коллоидную химию.
План лекции
1. Введение. Определения и сущность явлений изучаемых физической и коллоидной химией.
2. Введение в химическую термодинамику.
3. Понятия: система, параметры системы, функции состояния системы, термодинамические процессы.
4. Функции системы: внутренняя энергия и энтальпия. Математические выражения для них, их взаимосвязь.
5. 1 закон термодинамики – закон сохранения энергии.
6. 2 закон термодинамики. Однонаправленность процессов.
7. Свободная энергия системы. Самопроизвольные процессы.
Термин «физическая химия» и определение этой науки впервые были даны М.В. Ломоносовым. «Физическая химия есть наука, объясняющая на основании положений и опытов физики то, что происходит в смешанных телах при химических операциях».
Современное определение: Физическая химия – наука, объясняющая химические явления и устанавливающая их закономерности на основе общих принципов физики.
Современная физическая химия изучает много разнообразных явлений и, в свою очередь, разделяется на крупные, практически самостоятельные разделы области науки – электрохимию, фотохимию, химическую термодинамику и т. д. Но и сегодня основной задачей физической химии является изучение взаимосвязи физических и химических явлений.
Физическая химия-это не только теоретическая дисциплина. Знание законов физической химии позволяет понять сущность химических процессов и сознательно выбирать наиболее благоприятные условия для их практического осуществления. В основе многих процессов, протекающих при производстве металлов и их сплавов, получении пластмасс, химических волокон, удобрений, лекарственных препаратов, неорганических веществ, лежат законы физической химии.
Одним из разделов физической химии, который превратился в самостоятельную науку, является коллоидная химия. В коллоидной химии изучаются свойства систем, в которых одно вещество, находящееся в раздробленном (дисперсном) состоянии в виде частиц, состоящих из множества молекул, распределено в какой-либо среде (такие системы называются коллоидными). В коллоидную химию также в виде самостоятельного раздела входит физикохимия высокомолекулярных соединений или полимеров – природных (белка, целлюлозы, каучука и др.) и синтетических, имеющих молекулы очень больших размеров.
Большое значение физколлоидная химия имеет для пищевой технологии. Используемое для пищевой промышленности сырье и получаемые на предприятиях пищевой промышленности продукты питания в большинстве случаев являются или коллоидными системами, или ВМС. Такие распространенные в химии пищевой промышленности технологические операции как уваривание, сепарация, дистилляция, экстракция, кристаллизация и растворение, гидрирование могут быть поняты только на основе законов физической химии. Все биохимические процессы, лежащие в основе ряда пищевых производств, также подчиняются законам физической химии.
На методах физколлоидной химии основан и технохимический контроль пищевых производств: определение кислотности, содержание сахаров, жира, воды, витаминов, белков.
Химическая термодинамика
Термодинамика – раздел физической химии, в то ж время является самостоятельной наукой, которая
1) изучает законы взаимного превращения различных видов энергии при физических и химических процессах
2) определяет зависимость энергетического эффекта этих процессов от условий их протекания
3) позволяет установить принципиальную возможность самопроизвольного течения химической реакции в данных условиях.
В химической термодинамике рассматриваются основные термодинамические законы. Термодинамические законы позволяют предсказать не только принципиальную возможность протекания реакций при данных условиях, но и выход продукта и тепловой эффект реакции. Реакции, протекающие с выделением тепла, могут служить источниками тепловой энергии. Изучение энергетических эффектов дает информацию о строении соединения, межмолекулярных связях и реакционной способности.
Термодинамика использует следующие понятия:
Система – тело (группа тел), выделенное из окружающей среды (фактически или мысленно).
Фаза – совокупность однородных частей системы с одинаковыми свойствами и имеющих поверхность раздела с другими частями системы. Например, система вода-лед имеет один и тот же химический состав, но отличается плотностью, строением, свойствами, следовательно, это двухфазная система.
Системы бывают гомогенные – содержат одну фазу (например, воздух, жидкие растворы – нет поверхности раздела), гетерогенные – содержат несколько фаз.
Химически однородная система – система, все участки объема которой обладают одинаковым составом. Физически однородная система – все участки объема обладают одинаковыми свойствами.
Изолированная система не может обмениваться с окружающей средой веществом или энергией (теплотой или работой), т.е. объем и энергия изолированной системы - постоянны.
Неизолированная система – может обмениваться с окружающей средой веществом ли энергией.
Закрытая система – не обменивается с окружающей средой веществом, но может – энергией, объем системы – непостоянен.
Открытая система – система, свободная от всех ограничений.
Любая система в любой момент может находиться в каком-то определенном состоянии.
Состояние – это совокупность физических и химических свойств, характеризующих данную систему. Свойства могут быть интенсивные - не зависящие от количества вещества (Р,Т), и экстенсивные – зависящие от количества вещества (масса, объем).
При рассмотрении термодинамических свойств системы называют термодинамическими, такие системы характеризуются термодинамическими параметрами : температура, давление, объем, концентрация и др.
Так состояние равновесия в системе устанавливается при некоторых определенных сочетаниях термодинамических параметров. Математическое уравнение, показывающее взаимосвязь этих параметров для данной равновесной системы, называют уравнением состояния:
PV = nRT – Уравнение Менделеева-Клапейрона
Изменение хотя бы одного из параметров означает изменение состояния всей системы.
Термодинамический процесс – это любое изменение в системе, связанное с изменением хотя бы одного из параметров. Если изменение параметра не зависит от пути процесса, а зависит только от начального и конечного состояния системы, такое изменение называют функцией состояния . Процесс не зависит от пути протекания, а определяется начальным и конечным состоянием системы.
Круговой процесс или цикл - процесс, при котором термодинамическая система из начального состояния, претерпев ряд изменений, возвращается в первоначальное состояние. В таком процессе изменение любого параметра равно нулю.
Процессы могут иметь обратимый или необратимый характер.
Обратимый процесс – процесс, допускающий возможность возвращения в исходное первоначальное состояние.
Необратимый процесс – не означает, что этот процесс невозможно провести в обратном направлении. Необратимость означает. Что такое возвращение невозможно при помощи той же работы и энергии, с которыми процесс шел в прямом направлении.
I закон термодинамики:
- В любой изолированной системе сумма всех видов энергии постоянна.
- Разные формы энергии переходят друг в друга в строго эквивалентных количествах
- Вечный двигатель первого рода невозможен. Невозможно построить машину, которая давала бы механическую работу, не затрагивая на это соответствующего количества молекулярной энергии.
Первый закон термодинамики выражает неуничтожимость и эквивалентность различных форм энергии при различных переходах.
1 закон термодинамики представляет собой применение закона сохранения энергии к тепловым явлениям. Учитывая это можно его сформулировать в общем виде: Изменение внутренней энергии системы не зависит от пути процесса, а зависит только от начального и конечного состояния системы .
Математически это означает, что внутренняя энергия является функцией состояния, т.е. однозначные функции ряда переменных определяют это состояние.
Имеется система: газ, заключенный в поршневой цилиндр.
Эта система получает от нагревателя из окружающей среды определенное количество тепла. Часть подведенного тепла к системе будет затрачена на совершение работы против внешнего давления (работа расширения газа). При этом происходит увеличение объема газа. Оставшееся тепло будет затрачено на увеличение внутренней энергии системы – повышение температуры. При этом нив окружающей среде, ни в самой системе количество энергии не изменится.
Следовательно, сумма проведенной системой работы и прироста ее внутренней энергии должны быть равны количеству тепла, поступившего от нагревателя из окружающей среды:
Закон сохранения энергии выражает смысл первого начала термодинамики: Увеличение внутренней энергии системы равно сообщенному системе теплу минус работа, произведенная системой:
∆U = Q – A (2)
Формулы 1 и 2 – математические формулировки первого начала термодинамики.
Внутренняя энергия – это запас энергии системы, независимо от того, в каком состоянии она находится. Внутренняя энергия – общий запас энергии системы, которая складывается из энергии движения молекул, ядер и электронов в молекулах и атомах, энергии межмолекулярного взаимодействия. Из общего запаса энергии следует вычесть кинетическую энергию системы и потенциальную энергию ее положения. Для изолированной системы сумма всех видов энергии постоянная U = const. Обычно говорят об изменении внутренней энергии:
ΔU = U 2 – U 1
Изменение внутренней энергии системы может происходить:
1) в результате хаотического столкновения молекул двух соприкасающихся тел -мерой изменения энергии при этом является теплота
2) в результате совершения работы или самой системой или над системой: перемещение различных масс – поднятие тел в поле тяготения, переход электричеств от большего к меньшему потенциалу, расширение газа. Работа в этом случае также является мерой изменения энергии.
Следовательно, теплота –Q- и работа - A – количественно и качественно характеризуют формы передачи энергии (это меры энергии). U, A, Q – измеряются в одних и тех же единицах – кДж или кДж/моль.
Кроме внутренней существуют другие виды энергии: электромагнитная, электрическая, химическая, тепловая и т.д.
Другой вид энергии, который является также термодинамической функцией состояния–энтальпия –Н. Энтальпия - этомераэнергии,накапливаемая веществом при его образовании, это энергия расширенной системы, это теплосодержание системы . Математическое выражение для энтальпии:
Н = U + А
Т.е. энтальпия определяется внутренней энергией. Энтальпия и внутренняя энергия сильно отличаются друг от друга для газовых систем, но мало отличаются для конденсированных систем: жидких и твердых.
Поскольку энтальпия также является функцией состояния, т.е. всецело определяется начальным и конечным состоянием системы, то правильно говорить об изменении энтальпии системы:
ΔН = Н 2 – Н 1
ΔН = ΔU + А А = PΔV, где
P – давление; А – работа; ΔV – изменение объема.
PΔV – работа расширения
Энтальпия равна теплоте системы с обратным знаком.
Министерство образования и науки РФ
Санкт-Петербургский государственный политехнический университет
Факультет технологии и исследования материалов
Кафедра «Физической химии, микро- и нанотехнологий»
КУРСОВАЯ РАБОТА
«Термодинамическая оценка возможности протекания
химического процесса»
Вариант № 18
по дисциплине «Физическая химия»
Работу выполнил студент группы 2068/2
______________ / Дмитриева А.В.
Работу проверил
______________ / ст. преподаватель Елизарова Е.П.
Расчет провести, используя следующие приближения:
- Принять теплоемкости всех участников реакции.
- Принять.
- Принять.
Табличные данные, для всех участников реакции приведены ниже.
Вещество |
кДж/моль∙К |
||||||
В конце представить все расчетные данные в таблицу и на основе анализа полученных значений ответить на следующие вопросы:
- Определить термодинамическую вохможность протекания химической реакции при данной температуре.
- Установить с точки зрения термохимии тип данной реакции.
- Оценить влияние температуры и давления на величину и сдвиг равновесия.
Энтропийный метод расчета изменения энергии Гиббса и константы равновесия химической реакции
В данном методе используются значения энтропии веществ, участвующих в реакции. Он основан на соотношении
(где – изменение энергии
Гиббса при температуре Т;
тепловой эффект
реакции при температуре Т;
изменение энтропии
реакции при температуре Т) ,
выведенном из уравнения G = H – TS для реакции, протекающей при постоянной температуре. Так как стандартные значения энтропий и теплот образования веществ были определены при стандартных условиях (p= 1 атм, Т= 298 К), возможен расчет стандартного изменения энергии Гиббса по формуле:
Вначале определяют при температуре 298 К тепловой эффект реакции и алгебраическую сумму энтропий участников реакции с учетом стехиометрических коэффициентов:
Тепловой эффект реакции при заданной температуре рассчитывают по закону Кирхгофа: производная от теплового эффекта по температуре равна алгебраической сумме теплоемкостей веществ, участвующих в реакции
Если, то тепловой эффект возрастает при увеличении температуры; если, то он уменьшается.
Алгебраическую сумму энтропий реакции находят из уравнений
Окончательно для вычисления изменения энергии Гиббса получим
Если в исследуемом интервале участники реакции претерпевают фазовые превращения, то изменения энтольпии и энтропии нужно находить, разбивая интервал интегрирования на участки:
теплоемкости, соответствующие
фазе в данном интервале температур;
если теплота образования относится
к продукту реакции, то ставится знак “+”; если к
исходному веществу, то знак “”.
В первом приближении уравнение (*) упрощается за счет приравнивания суммы теплоемкостей к нулю. То есть мы пренебрегаем температурной зависимостью энтольпий и энтропий веществ:
При втором приближении теплоемкость принимают постоянной величиной, равной теплоемкости веществ при Т=298 К и находят их алгебраическую сумму с учетом стехиометрических коэффициентов:
Тогда из формулы (*) получаем приближенную формулу:
Наиболее точное третье приближение учитывает температурную зависимость энтольпии и энтропии веществ, и расчет ведется по формуле (*).
Стандартное изменение энергии Гиббса позволяет определить главную характеристику химической реакции – константу химического равновесия.
Каждая химическая реакция через некоторое время после ее начала приходит в равновесное состояние. Равновесным называют такое состояние, при котором состав системы со временем не изменяется. Равновесие реакции будет характеризоваться константой равновесия. Наибольшее практическое значение имеют константы, выраженные через парциальные давления.
Если все вещества, участвующие в реакции, находятся в стандартных состояниях, то в этом случае
Вычислив численное значение константы равновесия, можно рассчитать выход любого продукта реакции и оценить оптимальные условая для проведения реакции (давление и температуру).
Также зная знак стандартного изменения энергии Гиббса, можно произвести оценку термодинамической вероятности протекания реакции. Если, то реакция может самопроизвольно протекать при данных условиях. Если, то реакция при заданных условиях не протекает.
Расчетная часть
Тепловой эффект реакции при Т=298 К:
Изменение энтропии реакции при Т=298 К:
Первое приближение (:
Теплоемкости веществ, участвующих в реакции, при Т=298 К:
Алгебраическая сумма теплоемкостей при Т=298 К:
Тогда изменение теплового эффекта и энтропии реакции при Т=1800 К:
Второе приближение (
В третьем приближении будем учитывать фазовые переходы, в данной реакции – плавление марганца. Тогда весь температурный отрезок 298-1800К разбиваем на два отрезка: до температуры плавления и после нее, и считаем теплоемкость веществ функцией, зависящей от температуры.
Для интервала температур 298 – 1517 К:
Для интервала 1517 – 1800 К:
Значения изнемения теплового эффекта реакции и изменение энтропии реакции с учетом фазового перехода:
Третье приближение (
Определим константу равновесия реакции для трех приближений:
Таблица расчетных данных.
- Во всех приближениях расчетное значение изменения энергии Гиббса положительно. Это значит, что реакция при температуре 1800К протекать не может.
- Изменение теплового эффекта реакции также во всех приближениях положительно, значит реакция является эндотермической и идет с поглощением теплоты.
- а) Влияние температуры на константу равновесия:
откуда видно, что при повышении температуры константа равновесия будет увеличиваться, и соответственно, равновесие будет смещаться в сторону продуктов реакции.
б) Влияние давления на константу равновесия:
где Const – некоторая величина; изменение молярного объема в результате реакции.
причем, то есть при повышении давления в системе константа равновесия будет увеличиваться, и равновесие семстится в сторону продуктов реакции.
Рассмотренные факторы обобщают принцип смещения равновесия, называемый также принципом Ле Шателье: если на систему, находящуюся в состоянии истинного равновесия, оказывается внешнее воздействие, то в системе возникает самопроизвольный процесс, компенсирующий данное воздействие.
Литература:
- А.Г.Морачевский, И.Б.Сладков. Руководство к выполнению термодинамических расчетов. – Л.: ЛПИ, 1975.
- А.П.Рузинов, Б.С.Гульницкий. Равновесные превращения химических реакций. – М.: Металлургия, 1976.
1.3РЕШЕНИЕ ТИПОВЫХ ЗАДАЧ ПО ТЕМЕ “ХИМИЧЕСКАЯ
ТЕРМОДИНАМИКА И ТЕРМОХИМИЯ”
(для нехимических специальностей)
1. Рассчита
й
те
Δ
H
o
298
химическо
й
реак
ц
ии
Na 2 O(т)
+ H 2 O(ж)
→
2NaOH(т)
по значениям стандартных теплот
образования веществ ( ,
см.
таблицу 1 приложения). Укажите тип реак
ц
и
(экзо-
или
эндотермическая).
Решение
Решение.
Используя справочные данные :S
o (NaOH,т
) =
64,16 Дж/(моль
·
К),
S
o (Na 2 O,т)
=
75,5 Дж/(моль
·
К),S
o (H 2 O,ж)
= 70 Дж/(моль
·
К),рассчитываем
Δ
S
o
298
:
Δ
S
o
298
= 2
·
S
o
(NaOH
,
т
) - [S
o (Na 2 O,
т
) + S
o (H 2 O,
ж
)] = 2
·
64,16
- (75,5 + 70) =
= - 17,18
Дж
/
К
.
Ответ: -17,18 Дж/К.
4. Рассчита
й
те
изменение энергии Гиббса (Δ
G
o
298
) для
проц
есса
Na 2 O(т) + H 2 O(ж)
→
2NaOH(т)по
значениям
стандартных энергий Гиббса образования веществ (см. таблицу 1
приложения).
Возможно ли самопроизвольное протекание реакции при стандартных
условиях и 298К ?
Решение:
При стандартных условиях и T=298К Δ G o 298 можно рассчитать как разность суммарной энергии Гиббса образования продуктов реакции и суммарной энергии Гиббса образования исходных веществ. Необходимые справочные данные : (NaOH,т ) = -381,1 кДж/моль, (Na 2 O) = -378 кДж/моль, (H 2 O,ж) = -237 кДж/моль.
Δ
G
o
298
= 2
·
(NaOH,т
)
- [ (Na 2 O,т)
+ (H 2 O,ж)]
= 2
·
(-381,1) -
- [-378 + (-237)] = -147,2 кДж.
Значение Δ G o 298 отрицательно, поэтому самопроизвольное протекание реакции возможно.
Ответ:-147,2 кДж;возможно.
5. Определите, возможно ли при 95 o С самопроизвольное протекание проц есса Na 2 O(т) + H 2 O(ж) → 2NaOH(т).Ответ обосну й те, рассчитав величину изменения энергии Гиббса при данно й температуре.
Решение:
Переведем температуру в шкалу Кельвина: Т =273+95=368К. Для расчета Δ G o 368 воспользуемся уравнением:
Δ G o 368 = Δ H o - T Δ S o
Воспользуемся изменениями энтальпии и энтропии , рассчитанными для данного процесса в предыдущих задачах. При этом величину изменения энтропии необходимо перевести изДж/К вкДж/К,поскольку значения Δ H и Δ G обычно измеряют в кДж.
17,18 Дж/К = -0,01718 кДж/К
Δ G o 368 = -153,6 - 368 · (-0,01718) = -147,3 кДж.
Таким образом, Δ G o 368 < 0, поэтому самопроизвольное протекание данного процесса при 95 o С возможно.
Ответ:-147,3 кДж;возможно.
6. Составьте термохимическое уравнение реакции взаимодействия Na 2 O(т) и H 2 O(ж), если при этом образуется 1 моль NaOH (т). В ответе приведите количество теплоты, указанное в термохимическом уравнении.
Решение:
Коэффициенты в термохимическом уравнении имеют смысл молей. Поэтому допустимы дробные значения коэффициентов. 1 моль гидроксида натрия может образоваться из 1/2 моля оксида натрия и 1/2 моля воды. В задании 1 (см. выше) рассчитано, что при образовании 2 моль NaOH
Федеральное агентство по образованию
Ангарская государственная техническая академия
Кафедра химии
Курсовая работа
по дисциплине «Химия»
Тема:
Определение термодинамической возможности
протекания химических процессов в реакции:
Исполнитель: *********.
студентка группы ЭУПу-08-10
Руководитель:
доцент кафедры химии
Кузнецова Т.А.
Ангарск 2009
Задание к курсовой работе
1. Привести физико-химическую характеристику всех участников реакции и способов их получения.
4. Определить возможность протекания реакции H 2+ Cl 2=2 HCl при стандартных условиях и при температуре = 1000 К.
5. Используя метод Темкина-Шварцмана рассчитать
при температуре = 1200, =1500. Построив зависимость графически определить температуру, при которой процесс возможен, как самопроизвольный в прямом направлении. = 1200, =1500.
1. Теоретическая часть
1.1 Этанол и его свойства
Этанол – бесцветная подвижная жидкость с характерным запахом и жгучим вкусом.
Таблица 1. Физические свойства этанола
Смешивается с водой, эфиром, ацетоном и многими другими органическими растворителями; легко воспламеняется; с воздухом этанол образует взрывоопасные смеси (3,28-18,95% по объему). Этанол обладает всеми характерными для одноатомных спиртов химическими свойствами, например с щелочными и щелочноземельными металлами образует алкоголяты, с кислотами – сложные эфиры, при окислении этанола – ацетальдегид, при дегидратации – этилен и этиловый эфир. При хлорировании этанола образуется хлораль.
1.2 Способы получения этанола
Существует 2 основных способа получения этанола - микробиологический (брожение и гидролиз ) и синтетический:
Брожение
Известный с давних времён способ получения этанола - спиртовое брожение органических продуктов, содержащих сахар (свёкла и т. п.). Аналогично выглядит переработка крахмала, картофеля, риса, кукурузы, древесины и др. под действием фермента зимазы. Реакция эта довольно сложна, её схему можно выразить уравнением:
C 6 H 12 O 6 → 2C 2 H 5 OH + 2CO 2
В результате брожения получается раствор, содержащий не более 15 % этанола, так как в более концентрированных растворах дрожжи обычно гибнут. Полученный таким образом этанол нуждается в очистке и концентрировании, обычно путем дистилляции.
Промышленное производство спирта из биологического сырья
· Винокуренные заводы
· Гидролизное производство
Для гидролизного производства применяется сырьё, содержащее целлюлозу – древесина, солома.
· Отходами бродильного производства являются барда и сивушные масла
Гидратация этилена
В промышленности, наряду с первым способом, используют гидратацию этилена. Гидратацию можно вести по двум схемам:
· прямая гидратация при температуре 300 °C, давлении 7 МПа, в качестве катализатора применяют ортофосфорную кислоту, нанесённую на силикагель, активированный уголь или асбест:
CH 2 =CH 2 + H 2 O → C 2 H 5 OH
· гидратация через стадию промежуточного эфира серной кислоты, с последующим его гидролизом (при температуре 80-90 °С и давлении 3,5 МПа):
CH 2 =CH 2 + H 2 SO 4 → CH 3 -CH 2 -OSO 2 OH (этилсерная кислота)
CH 3 -CH 2 -OSO 2 OH + H 2 O → C 2 H 5 OH + H 2 SO 4
Эта реакция осложняется образованием диэтилового эфира.
Очистка этанола
Этанол, полученный путём гидратации этилена или брожением, представляет собой водно-спиртовую смесь, содержащую примеси. Для его промышленного, пищевого и фармакопейного применения необходима очистка. Фракционная перегонка позволяет получить этанол с концентрацией около 95.6 % об.; эта неразделимая перегонкой азеотропная смесь содержит 4.4 % воды (вес.) и имеет температуру кипения 78.2 °C.
Перегонка освобождает этанол как от легколетучих, так и от тяжёлых фракций органических веществ (кубовый остаток).
Абсолютный спирт
Абсолютный спирт - этиловый спирт, практически не содержащий воды. Кипение при температуре 78,39 °C в то время как спирт спирт-ректификат, содержащий не менее 4,43 % воды кипит при температуре 78,15 °C. Получают перегонкой водного спирта, содержащего бензол, и другими способами.
1.3 Применение
Топливо
Этанол может использоваться как топливо (в т. ч. для ракетных двигателей, двигателей внутреннего сгорания).
Химическая промышленность
· Служит сырьём для получения многих химических веществ, таких, как ацетальдегид, диэтиловый эфир, тетраэтилсвинец, уксусная кислота, хлороформ, этилацетат, этилен и др.;
· Широко применяется как растворитель (в красочной промышленности, в производстве товаров бытовой химии и многих других областях);
· Является компонентом антифриза.
Медицина
Этиловый спирт в первую очередь используется как антисептик
· как обеззараживающее и подсушивающее средств, наружно;
· растворитель для лекарственных средств, для приготовления настоек, экстрактов из растительного сырья и др.;
· консервант настоек и экстрактов (минимальная концентрация 18 %)
Парфюмерия и косметика
Является универсальным растворителем различных душистых веществ и основным компонентом духов, одеколонов и т. п. Входит в состав разнообразных лосьонов.
Пищевая промышленность
Наряду с водой, является необходимым компонентом спиртных напитков (водка, виски, джин и др.). Также в небольших количествах содержится в ряде напитков, получаемых брожением, но не причисляемых к алкогольным (кефир, квас, кумыс, безалкогольное пиво и др.). Содержание этанола в свежем кефире ничтожно (0,12 %), но в долго стоявшем, особенно в тёплом месте, может достичь 1 %. В кумысе содержится 1−3 % этанола (в крепком до 4,5 %), в квасе - от 0,6 до 2,2 %. Растворитель для пищевых ароматизаторов. Применяется как консервант для хлебобулочных изделий, а также в кондитерской промышленности
1.4 Этилен. Физические и химические свойства
Этилен , H2C=CH2 – ненасыщенный углеводород, первый член гомологического ряда олефинов, бесцветный газ со слабым эфирным запахом; практически нерастворим в воде, плохо - в спирте, лучше - в эфире, ацетоне. Горит слабокоптящим пламенем, с воздухом образует взрывоопасные смеси. Этилен весьма реакционноспособен.
Таблица 2. Физические свойства этилена