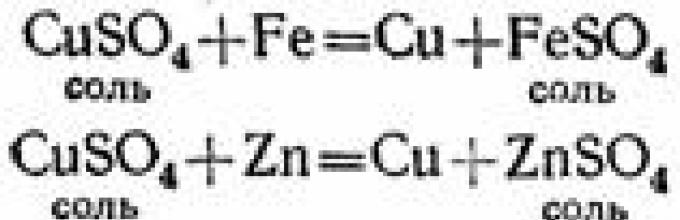СОЛИ, продукты замещения атомов водорода кислоты на металл или другой катион либо HО групп оснований на кислотный остаток или другой анион. По растворимости в воде различают растворимые, мало растворимые и практически нерастворимые соли. Сырьем… … Современная энциклопедия
Соли - СОЛИ, продукты замещения атомов водорода кислоты на металл или другой катион либо HО–групп оснований на кислотный остаток или другой анион. По растворимости в воде различают растворимые, мало растворимые и практически нерастворимые соли. Сырьем… … Иллюстрированный энциклопедический словарь
СОЛИ - класс хим. соединений, в твёрдом состоянии кристаллические вещества, состоящие из катионов (см.) и анионов (см.), а в водном растворе диссоциирующие на эти (см.). С. являются продуктами полного млн. частичного замещения атомов водорода в молекуле … Большая политехническая энциклопедия
СОЛИ - СОЛИ, продукты замещения ионов водорода. в к тах ионами металлов; могут быть получены разными способами: 1) замещением водорода к ты металлом, напр. Zn + H2S04=ZnS04 fH2, или вытеснением в С. одного металла другим: CuS04 +Fo =FeS04 + Си; 2)… … Большая медицинская энциклопедия
Солить(ся), солю, солишь, солят(ся) … Русское словесное ударение
Соледар Географические названия мира: Топонимический словарь. М: АСТ. Поспелов Е.М. 2001 … Географическая энциклопедия
Продукты замещения атомов водорода кислоты на металл или групп ОН основания на кислотный остаток. При полном замещении образуются средние, или нормальные, соли (NaCl, K2SO4 и др.), при неполном замещении атомов Н кислые (напр., NaHCO3), неполном … Энциклопедический словарь
Соли - класс химических соединений; в обычных условиях кристаллические вещества, для которых типична ионная структура. Соли в растворах диссоциируются на положительно заряженные ионы катионы (в основном металлов) и отрицательно заряженн ионы… … Энциклопедический словарь по металлургии
Солю, солишь и солишь; прич. страд. прош. соленный, лен, а, о; несов. 1. (сов. посолить) перех. Сыпать соль в какое л. или на какое л. кушанье, приправлять солью. Солить суп. Солить хлеб. □ Воробьев ел что придется, рассеянно солил и перчил,… … Малый академический словарь
соли - СОЛИ, ей, мн Спец. Химическое соединение, вещество, представляющее собой продукт полного или частичного замещения водорода кислоты металлом. Многие соли растворимы в воде … Толковый словарь русских существительных
Книги
- Спор о соли и железе (Янь те лунь). Том II , Хуань Куань. В древнекитайском памятнике, важнейшем источнике сведений об идеологии, истории и культуре Западной Хань (II-I вв. до н. э.), в форме дискуссии (спора) приведены точки зрения высших…
- 299рецептов заготовок без соли и сахара , А. А. Синельникова. Домашние заготовки, приготовленные традиционным способом, содержат большое количество соли или сахара, которые вредны в определенных количествах и особенно – принекоторых заболеваниях. Свежие… электронная книга
Соли - сложные вещества, состоящие из атома металла, или иона аммония NH + 4 и кислотного остатка (иногда содержат водород).
Практически все соли являются ионными соединениями, поэтому в солях между собой связаны ионы кислотных остатков и ионы металла
Соли - твердые кристаллические вещества. Многие вещества имеют высокие температуры плавления и кипения. По растворимости делятся на растворимые и нерастворимые.
Соль является продуктом частичного или полного замещения металлом атомов водорода кислоты. Отсюда различают следующие виды солей:
1. Средние соли
– все атомы водорода в кислоте замещены металлом: Na 2 CO 3 , KNO 3 и т.д.
2. Кислые соли
– не все атомы водорода в кислоте замещены металлом. Разумеется, кислые соли могут образовывать только двух- или многоосновные кислоты. Одноосновные кислоты кислых солей давать не могут: NaHCO 3 , NaH 2 PO 4 ит. д.
3. Двойные соли – атомы водорода двух- или многоосновной кислоты замещены не одним металлом, а двумя различными: NaKCO 3 , KAl(SO 4) 2 и т.д.
4. Соли основные можно рассматривать как продукты неполного, или частичного, замещения гидроксильных групп оснований кислотными остатками: Аl(OH)SO 4 , Zn(OH)Cl и т.д.
КЛАССИФИКАЦИЯ СОЛЕЙ
Химические свойства
1. B водных растворах соли могут реагировать со щелочами .
(хлористый магний MgCl2 взаимодействует с едким натром, образуя новую соль и новое основание: )
2. Соли могут реагировать с кислотами. Так, раствор азотнокислого бария
взаимодействует с раствором серной кислоты, образуя новую кислоту и
новую соль:
З. В водных растворах соли могут реагировать между собой.
Если слить вместе водные растворы хлористого кальция CaCl2 и углекислого натрия Na2CO3, TO образуется белый осадок нерастворимого в воде углекислого кальция СаСО3, а в растворе - хлористый натрий:
4. В водных растворах солей металл, входящий в их состав, может замещаться другим металлом, стоящим до него в ряду активности.
Если в раствор сернокислой меди опустить чистую железную проволоку или кусочек цинка, то на их поверхности выделяется медь, а в растворе образуется сернокислое железо (если было опущено железо) или сернокислый цинк (если был опущен цинк):

Запомнить!!!
1. Соли реагируют
со щелочами (если выпадает осадок или выделяется газ аммиак)
с кислотами, более сильными, чем та, которой образована соль
с другими растворимыми солями (если выпадает осадок)
с металлами (более активные вытесняют менее активные)
с галогенами (более активные галогены вытесняют менее активные и серу)
2. Нитраты разлагаются с выделением кислорода:
если металл стоит до Mg, образуется нитрит + кислород
если металл от Mg до Cu, образуется оксид металла + NO2 + O2
если металл стоит после Cu, образуется металл + NO2 + O2
нитрат аммония разлагается на N2O и H2O
3. Карбонаты щелочных металлов не разлагаются при нагревании
4. Карбонаты металлов II группы разлагаются на оксид металла и углекислый газ
Билет 11. Соляная кислота (Хлоридна кислота). Хлориды. Химические свойства.
Билет 18. Типы химической связи. Ионный и ковалентный. Примеры.
Солями называются сложные вещества, молекулы которых, состоят из атомов металлов и кислотных остатков (иногда могут содержать водород). Например, NaCl – хлорид натрия, СаSO 4 – сульфат кальция и т. д.
Практически все соли являются ионными соединениями, поэтому в солях между собой связаны ионы кислотных остатков и ионы металла:
Na + Cl – – хлорид натрия
Ca 2+ SO 4 2– – сульфат кальция и т.д.
Соль является продуктом частичного или полного замещения металлом атомов водорода кислоты. Отсюда различают следующие виды солей:
1. Средние соли – все атомы водорода в кислоте замещены металлом: Na 2 CO 3 , KNO 3 и т.д.
2. Кислые соли – не все атомы водорода в кислоте замещены металлом. Разумеется, кислые соли могут образовывать только двух- или многоосновные кислоты. Одноосновные кислоты кислых солей давать не могут: NaHCO 3 , NaH 2 PO 4 ит. д.
3. Двойные соли – атомы водорода двух- или многоосновной кислоты замещены не одним металлом, а двумя различными: NaKCO 3 , KAl(SO 4) 2 и т.д.
4. Соли основные можно рассматривать как продукты неполного, или частичного, замещения гидроксильных групп оснований кислотными остатками: Аl(OH)SO 4 , Zn(OH)Cl и т.д.
По международной номенклатуре название соли каждой кислоты происходит от латинского названия элемента. Например, соли серной кислоты называются сульфатами: СаSO 4 – сульфат кальция, Mg SO 4 – сульфат магния и т.д.; соли соляной кислоты называются хлоридами: NaCl – хлорид натрия, ZnCI 2 – хлорид цинка и т.д.
В название солей двухосновных кислот добавляют частицу «би» или «гидро»: Mg(HCl 3) 2 – бикарбонат или гидрокарбонат магния.
При условии, что в трехосновной кислоте замещён на металл только один атом водорода, то добавляют приставку «дигидро»: NaH 2 PO 4 – дигидрофосфат натрия.
Соли – это твёрдые вещества, обладающие самой различной растворимостью в воде.
 Химические свойства солей
Химические свойства солей
Химические свойства солей определяются свойствами катионов и анионов, которые входят в их состав.
1. Некоторые соли разлагаются при прокаливании:
CaCO 3 = CaO + CO 2
2. Взаимодействуют с кислотами с образованием новой соли и новой кислоты. Для осуществление этой реакции необходимо, чтобы кислота была более сильная чем соль, на которую воздействует кислота:
2NaCl + H 2 SO 4 → Na 2 SO 4 + 2HCl.
3. Взаимодействуют с основаниями , образуя новую соль и новое основание:
Ba(OH) 2 + Mg SO 4 → BaSO 4 ↓ + Mg(OH) 2 .
4. Взаимодействуют друг с другом с образованием новых солей:
NaCl + AgNO 3 → AgCl + NaNO 3 .
5. Взаимодействуют с металлами, которые стоят в раду активности до металла, который входит в состав соли:
Fe + CuSO 4 → FeSO 4 + Cu↓.
Остались вопросы? Хотите знать больше о солях?
Чтобы получить помощь репетитора – .
Первый урок – бесплатно!
blog.сайт, при полном или частичном копировании материала ссылка на первоисточник обязательна.
4. Классификация, получение и свойства солей
Наиболее сложными среди неорганических соединений являются соли. Они очень разнообразны по составу. Их делят на средние, кислые, основные, двойные, комплексные, смешанные.
Солями называются соединения, образующие при диссоциации в водном растворе положительно заряженные ионы металлов и отрицательно заряженные ионы кислотных остатков, а иногда, кроме них, ионы водорода и гидроксид-ионы.
Соли можно рассматривать как продукты замещения атомов водорода в кислоте атомами металлов (или группами атомов):
H 2 SO 4 → NaHSO 4 → Na 2 SO 4 ,
Или как продукты замещения гидроксогрупп в основном гидроксиде кислотными остатками:
Zn (OH ) 2 → ZnOHCl → ZnCl 2 .
При полном замещении получаются средние (или нормальные) соли:
Ca(OH) 2 + H 2 SO 4 = CaSO 4 + 2H 2 O.
При растворении средних солей образуются катионы металла и анионы кислотного остатка:
Na 2 SO 4 →2 Na + + SO 4 2 - .
При неполном замещении водорода кислоты получаются кислые соли :
NaOH + H 2 CO 3 = NaHCO 3 + H 2 O .
При растворении кислых солей в растворе образуются катионы металла, сложные анионы кислотного остатка, а также ионы, являющиеся продуктами диссоциации этого сложного остатка, в том числе ионы Н + :
NaHCO 3 →Na + + HCO 3 -
HCO 3 - H + + CO 3 2 - .
При неполном замещении гидроксогрупп основания - основные соли :
Mg(OH) 2 + HBr = Mg(OH)Br + H 2 O.
При растворении основных солей в растворе образуются анионы кислоты и сложные катионы, состоящие из металла и гидроксогрупп. Эти сложные катионы также способны к диссоциации. Поэтому в растворе основной соли присутствуют ионы ОН - :
Mg(OH)Br → (MgOH) + + Br - ,
(MgOH ) + Mg 2+ + OH - .
Таким образом, в соответствии с данным определением, соли делятся на средни е, кислые и основные .
Существуют также некоторые другие типы солей, например: двойные соли, в которых содержатся два разных катиона и один анион: CaCO 3 × MgCO 3 (доломит), KCl ∙ NaCl (сильвинит), KAl (SO 4 ) 2 (алюмокалиевые квасцы); смешанные соли , в которых содержится один катион и два разных аниона: CaOCl 2 (или CaCl (OCl )) - кальциевая соль соляной и хлорноватистой ( HOCl ) кислот (хлорид-гипохлорит кальция). Комплексные соли содержат комплексные катионы или анионы: K 3 + [ Fe (CN ) 6 ] −3 , K 4 + [ Fe (CN ) 6 ] −4 , [ Cr (H 2 O ) 5 Cl ] 2+ Cl 2 − .
Согласно современным номенклатурным правилам, названия солей образуются из названия аниона в именительном падеже и названия катиона в родительном падеже. Например FeS - сульфид железа ( II ), Fe 2 (SO 4 ) 3 - сульфат железа ( III ). Атом водорода, входящий в состав кислой соли, обозначается приставкой гидро - ( NaHSO 3 -гидросульфит натрия), а группа ОН - - приставкой гидроксо - ( Al (OH ) 2 Cl - дигидроксохлорид алюминия).
Получение солей
Соли тесно связаны со всеми остальными классами неорганических соединений и могут быть получены практически из любого класса. Большинство способов получения солей уже было обсуждено выше (разд. , ), к ним относятся:
1. Взаимодействие основных, кислотных и амфотерных оксидов друг с другом:
BaO + SiO 2 = BaSiO 3 ,
MgO + Al 2 O 3 = Mg(AlO 2) 2 ,
SO 3 + Na 2 O = Na 2 SO 4 ,
P 2 O 5 + Al 2 O 3 = 2AlPO 4 .
2. Взаимодействие оксидов с гидроксидами (с кислотами и основаниями):
ZnO + H 2 SO 4 = ZnSO 4 + H 2 O,
CO 2 + 2KOH = K 2 CO 3 + H 2 O,
2 NaOH + Al 2 O 3 = 2 NaAlO 2 + H 2 O .
3. Взаимодействие оснований со средними и кислыми солями:
CuSO 4 + 2KOH = Cu(OH) 2 ↓ + K 2 SO 4 ,
K 2 SO 4 + Ba(OH) 2 = 2KOH + BaSO 4 ↓ .
2NaHSO 3 + 2KOH = Na 2 SO 3 + K 2 SO 3 +2H 2 O,
Ca(HCO 3) 2 + Ba(OH) 2 = BaCO 3 ↓ + CaCO 3 ↓ + 2H 2 O.
Cu(OH) 2 + 2NaHSO 4 = CuSO 4 + Na 2 SO 4 +2H 2 O.
4. Соли бескислородных кислот, кроме того, могут быть получены при непосредственном взаимодействии металлов и неметаллов:
2 Mg + Cl 2 = MgCl 2 .
Химические свойства солей
При химических реакциях солей проявляются особенности как катионов, так и анионов, входящих в их состав. Катионы металлов, находящиеся в растворах, могут вступать в реакции с другими анионами с образованием нерастворимых соединений. С другой стороны, анионы, входящие в состав солей, могут соединяться с катионами с образованием осадков или малодиссоциированных соединений (или же в окислительно-восстановительные реакции). Таким образом, соли могут реагировать:
|
1. С металлами |
Cu + HgCl 2 = CuCl 2 + Hg , Zn + Pb(NO 3) 2 = Zn(NO 3) 2 + Pb. |
|
2. C кислотами |
Na 2 CO 3 + 2HCl = 2NaCl + H 2 O + CO 2 , AgCl + HBr = AgBr ↓ + HCl |
|
3. C солями |
AgNO 3 + NaCl = AgCl ↓ + NaNO 3 , K 2 CrO 4 + Pb(NO 3) 2 = KNO 3 + PbCrO 4 ↓ . |
|
4. C основаниями |
CuSO 4 + 2NaOH = Cu(OH) 2 ↓ + Na 2 SO 4 , Ni(NO 3) 2 + 2KOH = Ni(OH) 2 + 2KNO 3 . |
|
5. Многие соли устойчивы при нагревании. Однако, соли аммония, а также некоторые соли малоактивных металлов, слабых кислот и кислот, в которых элементы проявляют высшие или низшие степени окисления, при нагревании разлагаются: CaCO 3 = CaO + CO 2 , 2Ag 2 CO 3 = 4Ag + 2CO 2 + O 2 , NH 4 Cl = NH 3 + HCl, 2KNO 3 = 2KNO 2 + O 2 , 2FeSO 4 = Fe 2 O 3 + SO 2 + SO 3 , 4FeSO 4 = 2Fe 2 O 3 + 4SO 2 + O 2 , NH 4 NO 3 = N 2 O + 2 H 2 O . |
|
М.В. Андрюxoва, Л.Н. Бopoдина
Рассмотрим важнейшие способы получения солей.
Реакция нейтрализации . Растворы кислоты и основания смешивают в нужном мольном соотношении. После выпаривания воды получают кристаллическую соль. Например:
2 . Реакция кислот с основными оксидами . Фактически, это вариант реакции нейтрализации. Например:
3 . Реакция оснований с кислотными оксидами . Это также вариант реакции нейтрализации:
4 . Реакция основных и кислотных оксидов между собой :
5 . Реакция кислот с солями . Этот способ подходит, например, в том случае, если образуется нерастворимая соль, выпадающая в осадок:
6 . Реакция оснований с солями . Для таких реакций подходят только щелочи (растворимые основания). В этих реакциях образуется другое основание и другая соль. Важно, чтобы новое основание не было щелочью и не могло реагировать с образовавшейся солью. Например:
7. Реакция двух различных солей. Реакцию удается провести только в том случае, если хотя бы одна из образующихся солей нерастворима и выпадает в осадок:
Выпавшую в осадок соль отфильтровывают, а оставшийся раствор упаривают и получают другую соль. Если же обе образующиеся соли хорошо растворимы в воде, то реакции не происходит: в растворе существуют лишь ионы, не взаимодействующие между собой:
NaCl + KBr = Na + + Cl + K + + Br
Если такой раствор упарить, то мы получим смесь солей NaCl, KBr, NaBr и KCl, но чистые соли в таких реакциях получить не удается.
8 . Реакция металлов с кислотами . Соли образуются и в окислительно-восстановительных реакциях. Например, металлы, расположенные левее водорода в ряду активности металлов (таблица 4-3), вытесняют из кислот водород и сами соединяются с ними, образуя соли:
9 . Реакция металлов с неметаллами . Эта реакция внешне напоминает горение. Металл «сгорает» в токе неметалла, образуя мельчайшие кристаллы соли, которые выглядят, как белый «дым»:
10 . Реакция металлов с солями . Более активные металлы, расположенные в ряду активности левее , способны вытеснять менее активные (расположенные правее ) металлы из их солей:
Рассмотрим химические свойства солей.
Наиболее распространенные реакции солей – реакции обмена и окислительно-восстановительные реакции. Сначала рассмотрим примеры окислительно-восстановительных реакций.
1 . Окислительно-восстановительные реакции солей .
Поскольку соли состоят из ионов металла и кислотного остатка, их окислительно-восстановительные реакции условно можно разбить на две группы: реакции за счет иона металла и реакции за счет кислотного остатка, если в этом кислотном остатке какой-либо атом способен менять степень окисления.
А) Реакции за счет иона металла.
Поскольку в солях содержится ион металла в положительной степени окисления, они могут участвовать в окислительно-восстановительных реакциях, где ион металла играет роль окислителя. Восстановителем чаще всего служит какой-нибудь другой (более активный) металл:
Принято говорить, что более активные металлы способны вытеснять другие металлы из их солей. Металлы, находящиеся в ряду активности левее (см. параграф 8.3), являются более активными.
Б) Реакции за счет кислотного остатка.
В кислотных остатках часто имеются атомы, способные изменять степень окисления. Отсюда –многочисленные окислительно-восстановительные реакции солей с такими кислотными остатками. Например:
|
соль иодоводородной кислоты | |||||||||||||||
|
соль марганцевой кислоты |
хлорид марганца | |||||||||
2 . Обменные реакции солей .
Такие реакции могут происходить, когда соли реагируют: а) с кислотами, б) с щелочами, в) с другими солями. При проведении обменных реакций берут растворы солей. Общим требованием для таких реакций является образование малорастворимого продукта, который удаляется из раствора в виде осадка. Например:
а) CuSO 4 + H 2 S = CuS↓ (осадок) + H 2 SO 4
AgNO 3 + HCl = AgCl↓ (осадок) + HNO 3
б) FeCl 3 + 3 NaOH = Fe(OH) 3 ↓ (осадок) + 3 NaCl
CuSO 4 + 2 KOH = Cu(OH) 2 ↓ (осадок) + K 2 SO 4
в) BaCl 2 + K 2 SO 4 = BaSO 4 ↓ (осадок) + 2 KCl
CaCl 2 + Na 2 CO 3 = CaCO 3 ↓ (осадок) + 2 NaCl
Если хотя бы один продукт таких обменных реакций не уходит из сферы реакции в виде осадка (иногда – в виде газа), то при смешивании растворов образуется только смесь ионов, на которые при растворении распадаются исходная соль и реагент. Таким образом, обменная реакция произойти не может.