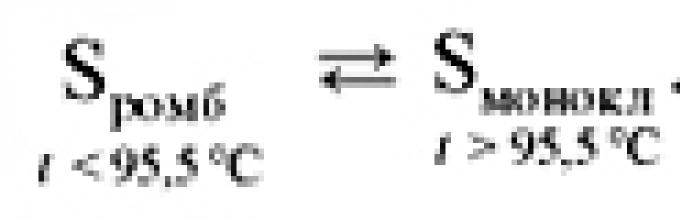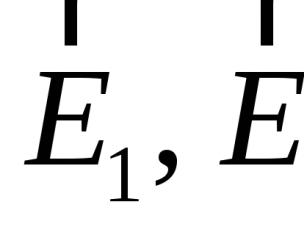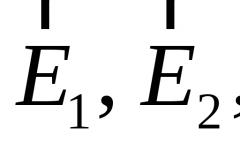Пособие-репетитор по химии
Продолжение. Cм. в № 22/2005;
1, 2, 3, 5, 6, 8, 9, 11, 13, 15, 16, 18, 22/2006;
3, 4, 7, 10, 11, 21/2007;
2, 7, 11, 18, 19, 21/2008;
1, 3, 10/2009
ЗАНЯТИЕ 30
10-й класс (первый год обучения)
Сера и ее соединения
1. Положение в таблице Д.И.Менделеева, строение атома.
2. Происхождение названия.
3. Физические свойства.
4. Химические свойства.
5. Нахождение в природе.
6. Основные методы получения.
7. Важнейшие соединения серы (сероводород, сероводородная кислота и ее соли; сернистый газ, сернистая кислота и ее соли; триоксид серы, серная кислота и ее соли).
В периодической системе сера находится в главной подгруппе VI группы (подгруппа халькогенов). Электронная формула серы 1s 2 2s 2 p 6 3s 2 p 4 , это р -элемент. В зависимости от состояния сера может проявлять валентность II, IV или VI:
S: 1s 2 2s 2 2p 6 3s 2 3p 4 3d 0 (валентность II),
S * : 1s 2 2s 2 2p 6 3s 2 3p 3 3d 1 (валентность IV),
S ** : 1s 2 2s 2 2p 6 3s 1 3p 3 3d 2 (валентность VI).
Характерные степени окисления серы –2, +2, +4, +6 (в дисульфидах, содержащих мостиковую связь –S–S– (например, FeS 2), степень окисления серы равна –1); в соединениях входит в состав анионов, с более электроотрицательными элементами – в состав катионов, например:
Сера – элемент с высокой электроотрицательностью, проявляет неметаллические (кислотные) свойства. Имеет четыре стабильных изотопа с массовыми числами 32, 33, 34 и 36. Природная сера на 95 % состоит из изотопа 32 S.
Русское название серы произошло от санскритского слова cira – светло-желтый, по цвету природной серы. Латинское название sulfur переводится как «горючий порошок». 1
Ф и з и ч е с к и е с в о й с т в а
Сера образует три аллотропные модификации : ромбическая (-сера), моноклинная (-сера) и пластическая , или каучукоподобная. Наиболее устойчива при обычных условиях ромбическая сера, а выше 95,5 °С стабильна моноклинная сера. Обе эти аллотропные модификации имеют молекулярную кристаллическую решетку, построенную из молекул состава S 8 , расположенных в пространстве в виде короны; атомы соединены одинарными ковалентными связями. Различие ромбической и моноклинной серы состоит в том, что в кристаллической решетке молекулы упакованы по-разному.
Если ромбическую или моноклинную серу нагреть до точки кипения (444,6 °С) и полученную жидкость вылить в холодную воду, то образуется пластическая сера, по свойствам напоминающая резину. Пластическая сера состоит из длинных зигзагообразных цепей. Эта аллотропная модификация неустойчива и самопроизвольно превращается в одну из кристаллических форм.
Ромбическая сера – твердое кристаллическое вещество желтого цвета; в воде не растворяется (и не смачивается), но хорошо растворяется во многих органических растворителях (сероуглерод, бензол и т.д.). Сера обладает очень плохой электро- и теплопроводностью. Температура плавления ромбической серы +112,8 °С, при температуре 95,5 °С ромбическая сера переходит в моноклинную:
![]()
Х и м и ч е с к и е с в о й с т в а
По своим химическим свойствам сера является типичным активным неметаллом. В реакциях может быть как окислителем, так и восстановителем.
![]()
Металлы (+):
2Na + S = Na 2 S,
2Al + 3S Al 2 S 3 ,
Неметаллы (+/–)*:
2P + 3S P 2 S 3 ,
S + Cl 2 = SCl 2 ,
S + 3F 2 = SF 6 ,
S + N 2 реакция не идет.
Н 2 О (–). сера не смачивается водой.
Основные оксиды (–).
Кислотные оксиды (–).
Основания (+/–):
S + Cu(OH) 2 реакция не идет.
Кислоты (не окислители) (–).
Кислоты-окислители (+):
S + 2H 2 SO 4 (конц.) = 3SO 2 + 2H 2 O,
S + 2HNO 3 (разб.) = H 2 SO 4 + 2NO,
S + 6HNO 3 (конц.) = H 2 SO 4 + 6NO 2 + 2H 2 O.
В п р и р о д е сера встречается как в самородном состоянии, так и в виде соединений, важнейшими из которых являются пирит, он же железный, или серный, колчедан (FeS 2), цинковая обманка (ZnS), свинцовый блеск (PbS), гипс (CaSO 4 2H 2 O), глауберова соль (Na 2 SO 4 10H 2 O), горькая соль (MgSO 4 7H 2 O). Кроме того, сера входит в состав каменного угля, нефти, а также в различные живые организмы (в составе аминокислот). В организме человека сера концентрируется в волосах.
В л а б о р а т о р н ы х у с л о в и я х серу можно получить, используя окислительно-восстановительные реакции (ОВР), например:
H 2 SO 3 + 2H 2 S = 3S + 3H 2 O,
2H 2 S + O 2 2S + 2H 2 O.
В а ж н е й ш и е с о е д и н е н и я с е р ы
Сероводород (H 2 S) – бесцветный газ с удушающим неприятным запахом тухлых яиц, ядовит (соединяется с гемоглобином крови, образуя сульфид железа). Тяжелее воздуха, малорастворим в воде (2,5 объема сероводорода в 1 объеме воды). Связи в молекуле ковалентные полярные, sp 3 -гибридизация, молекула имеет угловое строение:
В химическом отношении сероводород достаточно активен. Он термически неустойчив; легко сгорает в атмосфере кислорода или на воздухе; легко окисляется галогенами, диоксидом серы или хлоридом железа(III); при нагревании взаимодействует с некоторыми металлами и их оксидами, образуя сульфиды:
![]()
2H 2 S + O 2 2S + 2H 2 O,
2H 2 S + 3O 2 2SO 2 + 2H 2 O,
H 2 S + Br 2 = 2HBr + S,
2H 2 S + SO 2 3S + 2H 2 O,
2FeCl 3 + H 2 S = 2FeCl 2 + S + 2HCl,
H 2 S + Zn ZnS + H 2 ,
H 2 S + CaO CaS + H 2 O.
В лабораторных условиях сероводород получают действием на сульфиды железа или цинка сильных минеральных кислот или необратимым гидролизом сульфида алюминия:
ZnS + 2HCl = ZnCl 2 + H 2 S,
Аl 2 SO 3 + 6HOH 2Al(OH) 3 + 3H 2 S.
Раствор сероводорода в воде – сероводородная вода, или сероводородная кислота . Слабый электролит, по второй ступени практически не диссоциирует. Как двухосновная кислота образует два типа солей – сульфиды и гидросульфиды :
например, Na 2 S – сульфид натрия, NaHS – гидросульфид натрия.
Сероводородная кислота проявляет все общие свойства кислот. Кроме того, сероводород, сероводородная кислота и ее соли проявляют сильную восстановительную способность. Например:
H 2 S + Zn = ZnS + H 2 ,
H 2 S + CuO = CuS + H 2 O,

Качественной реакцией на сульфид-ион является взаимодействие с растворимыми солями свинца; при этом выпадает осадок сульфида свинца черного цвета:
Pb 2+ + S 2– -> PbS,
Pb(NO 3) 2 + Na 2 S = PbS + 2NaNO 3 .
Оксид серы(IV) SO 2 – сернистый газ, сернистый ангидрид – бесцветный газ с резким запахом, ядовит. Кислотный оксид. Связи в молекуле ковалентные полярные, sp 2 -гибридизация. Тяжелее воздуха, хорошо растворим в воде (в одном объеме воды – до 80 объемов SO 2), образует при растворении сернистую кислоту , существующую только в растворе:
H 2 O + SO 2 H 2 SO 3 .
По кислотно-основным свойствам сернистый газ проявляет свойства типичного кислотного оксида, сернистая кислота также проявляет все типичные свойства кислот:
SO 2 + CaO CaSO 3 ,

H 2 SO 3 + Zn = ZnSO 3 + H 2 ,

H 2 SO 3 + CaO = CaSO 3 + H 2 O.
По окислительно-восстановительным свойствам сернистый газ, сернистая кислота и сульфиты могут проявлять окислительно-восстановительную двойственность (с преобладанием восстановительных свойств). С более сильными восстановителями соединения серы(IV) ведут себя как окислители:
![]()
С более сильными окислителями они проявляют восстановительные свойства:
![]()
В промышленности диоксид серы получают:
При горении серы:
Обжигом пирита и других сульфидов:
4FeS 2 + 11O 2 2Fe 2 O 3 + 8SO 2 ,
2ZnS + 3O 2 2ZnO + 2SO 2 .
К лабораторным методам получения относятся:
Действие сильных кислот на сульфиты:
Na 2 SO 3 + 2HCl = 2NaCl + SO 2 + H 2 O;
Взаимодействие концентрированной серной кислоты с тяжелыми металлами:
Cu + 2H 2 SO 4 (конц.) = СuSO 4 + SO 2 + 2H 2 O.
Качественные реакции на сульфит-ион – обесцвечивание «йодной воды» или действие сильных минеральных кислот:
Na 2 SO 3 + I 2 + 2NaOH = 2NaI + Na 2 SO 4 + H 2 O,
Ca 2 SO 3 + 2HCl = CaCl 2 + H 2 O + SO 2 .
Оксид серы(VI) SO 3 – триоксид серы, или серный ангидрид , – это бесцветная жидкость, которая при температуре ниже 17 °С превращается в белую кристаллическую массу. Ядовит. Существует в виде полимеров (мономерные молекулы существуют только в газовой фазе), связи в молекуле ковалентные полярные, sp 2 -гибридизация. Гигроскопичен, термически неустойчив. С водой реагирует с сильным экзо-эффектом. Реагирует с безводной серной кислотой, образуя олеум . Образуется при окислении сернистого газа:
![]()
SO 3 + H 2 O = H 2 SO 4 + Q ,
n n SO 3 .
По кислотно-основным свойствам является типичным кислотным оксидом:
SO 3 + H 2 O = H 2 SO 4 ,
SO 3 + CaO = CaSO 4 ,

По окислительно-восстановительным свойствам выступает сильным окислителем, обычно восстанавливаясь до SO 2 или сульфитов:
![]()
В чистом виде практического значения не имеет, является промежуточным продуктом при производстве серной кислоты.
Серная кислота – тяжелая маслянистая жидкость без цвета и запаха. Хорошо растворима в воде (с большим экзо-эффектом). Гигроскопична, ядовита, вызывает сильные ожоги кожи. Является сильным электролитом. Серная кислота образует два типа солей: сульфаты и гидросульфаты , которые проявляют все общие свойства солей. Сульфаты активных металлов термически устойчивы, а сульфаты других металлов разлагаются даже при небольшом нагревании:
Na 2 SO 4 не разлагается,
ZnSO 4 ZnO + SO 3 ,
4FeSO 4 2Fe 2 O 3 + 4SO 2 + O 2 ,
Ag 2 SO 4 2Ag + SO 2 + O 2 ,
HgSO 4 Hg + SO 2 + O 2 .
Раствор с массовой долей серной кислоты ниже 70 % обычно считается разбавленным; выше 70 % – концентрированным; раствор SO 3 в безводной серной кислоте называется олеум (концентрация триоксида серы в олеуме может достигать 65 %).
Разбавленная серная кислота проявляет все свойства, характерные для сильных кислот:
Н 2 SO 4 2H + + SO 4 2– ,
Н 2 SO 4 + Zn = ZnSO 4 + Н 2 ,
Н 2 SO 4 (разб.) + Cu реакция не идет,
Н 2 SO 4 + CaO = CaSO 4 + H 2 O,

CaCO 3 + Н 2 SO 4 = CaSO 4 + H 2 O + CO 2 .
Концентрированная серная кислота является сильным окислителем, особенно при нагревании. Она окисляет многие металлы, неметаллы, а также некоторые органические вещества. Не окисляются под действием концентрированной серной кислоты железо, золото и металлы платиновой группы (правда, железо хорошо растворяется при нагревании в умеренно концентрированной серной кислоте с массовой долей 70 %). При взаимодействии концентрированной серной кислоты с другими металлами образуются сульфаты и продукты восстановления серной кислоты.
2Н 2 SO 4 (конц.) + Cu = CuSO 4 + SO 2 + 2H 2 O,

5Н 2 SO 4 (конц.) + 8Na = 4Na 2 SO 4 + H 2 S + 4H 2 O,
Н 2 SO 4 (конц.) пассивирует Fe, Al.
При взаимодействии с неметаллами концентрированная серная кислота восстанавливается до SO 2:
5Н 2 SO 4 (конц.) + 2Р = 2H 3 PO 4 + 5SO 2 + 2H 2 O,
2Н 2 SO 4 (конц.) + C = 2H 2 O + CO 2 + 2SO 2 .
Контактный метод получения серной кислоты состоит из трех стадий:
1) обжиг пирита:
4FeS 2 + 11O 2 2Fe 2 O 3 + 8SO 2 ;
2) окисление SO 2 в SO 3 в присутствии катализатора – оксида ванадия:
![]()
3) растворение SO 3 в серной кислоте с получением олеума:
SO 3 + H 2 O = H 2 SO 4 + Q ,
n SO 3 + H 2 SO 4 (конц.) = H 2 SO 4 n SO 3 .
Качественная реакция на сульфат-ион – взаимодействие с катионом бария, в результате чего выпадает белый осадок BaSO 4 .
Ba 2+ + SO 4 2– -> BaSO 4 ,
BaCl 2 + Na 2 SO 4 = BaSO 4 + 2NaCl.
Тест по теме «Сера и ее соединения»
1. Сера и кислород – это:
а) хорошие проводники электричества;
б) относятся к подгруппе халькогенов;
в) хорошо растворимы в воде;
г) имеют аллотропные модификации.
2. В результате реакции серной кислоты с медью можно получить:
а) водород; б) серу;
в) сернистый газ; г) сероводород.
3. Сероводород – это:
а) ядовитый газ;
б) сильный окислитель;
в) типичный восстановитель;
г) один из аллотропов серы.
4. Массовая доля (в %) кислорода в серном ангидриде равна:
а) 50; б) 60; в) 40; г) 94.
5. Оксид серы(IV) является ангидридом:
а) серной кислоты;
б) сернистой кислоты;
в) сероводородной кислоты;
г) тиосерной кислоты.
6. На сколько процентов уменьшится масса гидросульфита калия после прокаливания?
в) гидросульфит калия термически устойчив;
7. Сместить равновесие в сторону прямой реакции окисления сернистого газа в серный ангидрид можно:
а) используя катализатор;
б) увеличивая давление;
в) уменьшая давление;
г) понижая концентрацию оксида серы(VI).
8. При приготовлении раствора серной кислоты необходимо:
а) наливать кислоту в воду;
б) наливать воду в кислоту;
в) порядок приливания не имеет значения;
г) серная кислота не растворяется в воде.
9. Какую массу (в г) декагидрата сульфата натрия необходимо добавить к 100 мл 8%-го раствора сульфата натрия (плотность равна 1,07 г/мл), чтобы удвоить массовую долю соли в растворе?
а) 100; б) 1,07; в) 30,5; г) 22,4.
10. Для определения сульфит-иона в качественном анализе можно использовать:
а) катионы свинца;
б) «йодную воду»;
в) раствор марганцовки;
г) сильные минеральные кислоты.
Ключ к тесту
| б, г | в | а, в | б | б | г | б, г | а | в | б, г |
Задачи и упражнения на серу и ее соединения
Ц е п о ч к и п р е в р а щ е н и й
1. Сера -> сульфид железа(II) -> сероводород -> сернистый газ -> триоксид серы > серная кислота > оксид серы(IV).
3. Серная кислота -> сернистый газ -> сера -> диоксид серы -> триоксид серы -> серная кислота.
4. Сернистый ангидрид -> сульфит натрия -> гидросульфит натрия -> сульфит натрия -> сульфат натрия.
5. Пирит -> сернистый газ -> серный ангидрид -> серная кислота -> оксид серы(IV) -> сульфит калия -> сернистый ангидрид.
6. Пирит > сернистый газ -> сульфит натрия -> сульфат натрия -> сульфат бария -> сульфид бария.
7. Сульфид натрия -> А -> В -> С -> D -> сульфат бария (все вещества содержат серу; первая, вторая и четвертая реакции – ОВР).
| У р о в е н ь А |
1. Через раствор, содержащий 5 г едкого натра, пропустили 6,5 л сероводорода. Определите состав полученного раствора.
Ответ. 7 г NaHS, 5,61 г H 2 S.
2. Какую массу глауберовой соли необходимо добавить к 100 мл 8%-го раствора сульфата натрия (плотность раствора равна 1,07 г/мл), чтобы удвоить массовую долю вещества в растворе?
Ответ. 30,5 г Na 2 SO 4 10H 2 O.
3. К 40 г 12%-го раствора серной кислоты добавили 4 г серного ангидрида. Вычислите массовую долю вещества в образовавшемся растворе.
Ответ. 22 % H 2 SO 4 .
4. Смесь сульфида железа(II) и пирита, массой 20,8 г, подвергли длительному обжигу, при этом образовалось 6,72 л газообразного продукта (н.у.). Определите массу твердого остатка, образовавшегося при обжиге.
Ответ. 16 г Fe 2 O 3 .
5. Имеется смесь меди, углерода и оксида железа(III) с молярным соотношением компонентов 4:2:1 (в порядке перечисления). Какой объем 96%-й серной кислоты (плотность равна 1,84 г/мл) нужен для полного растворения при нагревании 2,2 г такой смеси?
Ответ. 4,16 мл раствора H 2 SO 4 .
6. Для окисления 3,12 г гидросульфита щелочного металла потребовалось добавить 50 мл раствора, в котором молярные концентрации дихромата натрия и серной кислоты равны 0,2 моль/л и 0,5 моль/л соответственно. Установите состав и массу остатка, который получится при выпаривании раствора после реакции.
Ответ . 7,47 г смеси сульфатов хрома (3,92 г) и натрия (3,55 г).
| У р о в е н ь Б |
(задачи на олеум)
1. Какую массу триоксида серы надо растворить в 100 г 91%-го раствора серной кислоты, чтобы получить 30%-й олеум?
Решение
По условию задачи:
m (H 2 SO 4) = 100 0,91 = 91 г,
m (H 2 O) = 100 0,09 = 9 г,
(H 2 O) = 9/18 = 0,5 моль.
Часть добавленного SO 3 (m 1) пойдет на реакцию с H 2 O:
H 2 O + SO 3 = H 2 SO 4 .
По уравнению реакции:
(SO 3) = (H 2 O) = 0,5 моль.
m 1 (SO 3) = 0,5 80 = 40 г.
Вторая часть SO 3 (m 2) пойдет на создание концентрации олеума. Выразим массовую долю олеума:

m 2 (SO 3) = 60 г.
Суммарная масса триоксида серы:
m (SO 3) = m 1 (SO 3) + m 2 (SO 3) = 40 + 60 = 100 г.
Ответ . 100 г SO 3 .
2. Какую массу пирита необходимо взять для получения такого количества оксида серы(VI), чтобы, растворив его в 54,95 мл 91%-го раствора серной кислоты (плотность равна 1,82 г/см 3), получить 12,5%-й олеум? Выход серного ангидрида считать за 75 %.
Ответ . 60 г FeS 2 .
3. На нейтрализацию 34,5 г олеума расходуется 74,5 мл 40%-го раствора гидроксида калия (плотность равна 1,41 г/мл). Сколько молей серного ангидрида приходится на 1 моль серной кислоты в этом олеуме?
Ответ . 0,5 моль SO 3 .
4. При добавлении оксида серы(VI) к 300 г 82%-го раствора серной кислоты получен олеум с массовой долей триоксида серы 10%. Найдите массу использованного серного ангидрида.
Ответ . 300 г SO 3 .
5. При добавлении 400 г триоксида серы к 720 г водного раствора серной кислоты получен олеум с массовой долей 7,14 %. Найдите массовую долю серной кислоты в исходном растворе.
Ответ . 90 % H 2 SO 4 .
6. Найдите массу 64%-го раствора серной кислоты, если при добавлении к этому раствору 100 г триоксида серы получается олеум, содержащий 20 % триоксида серы.
Ответ . 44,4 г раствора H 2 SO 4 .
7. Какие массы триоксида серы и 91%-го раствора серной кислоты необходимо смешать для получения 1 кг 20%-го олеума?
Ответ . 428,6 г SO 3 и 571,4 г раствора H 2 SO 4 .
8. К 400 г олеума, содержащего 20 % триоксида серы, добавили 100 г 91%-го раствора серной кислоты. Найдите массовую долю серной кислоты в полученном растворе.
Ответ . 92 % H 2 SO 4 в олеуме.
9. Найдите массовую долю серной кислоты в растворе, полученном при смешивании 200 г 20%-го олеума и 200 г 10%-го раствора серной кислоты.
Ответ . 57,25 % H 2 SO 4 .
10. Какую массу 50%-го раствора серной кислоты необходимо добавить к 400 г 10%-го олеума для получения 80%-го раствора серной кислоты?
Ответ . 296,67 г 50%-го раствора H 2 SO 4 .
Ответ . 114,83 г олеума.
К а ч е с т в е н н ы е з а д а ч и
1. Бесцветный газ А с резким характерным запахом окисляется кислородом в присутствии катализатора в соединение В, представляющее собой летучую жидкость. Вещество В, соединяясь с негашеной известью, образует соль С. Идентифицируйте вещества, напишите уравнения реакций.
Ответ . Вещества: А – SO 2 , B – SO 3 , C – CaSO 4 .
2. При нагревании раствора соли А образуется осадок В. Этот же осадок образуется при действии щелочи на раствор соли А. При действии кислоты на соль А выделяется газ С, обесцвечивающий раствор перманганата калия. Идентифицируйте вещества, напишите уравнения реакций.
Ответ . Вещества: А – Ca(HSO 3) 2 , B – CaSO 3 , C – SO 2 .
3. При окислении газа А концентрированной серной кислотой образуется простое вещество В, сложное вещество С и вода. Растворы веществ А и С реагируют между собой с образованием осадка вещества В. Идентифицируйте вещества, напишите уравнения реакций.
Ответ . Вещества: А – H 2 S, B – S, C – SO 2 .
4. В реакции соединения двух жидких при обычной температуре оксидов А и В образуется вещество С, концентрированный раствор которого обугливает сахарозу. Идентифицируйте вещества, напишите уравнения реакций.
Ответ . Вещества: А – SO 3 , B – H 2 O, C – H 2 SO 4 .
5. В вашем распоряжении имеются сульфид железа(II), сульфид алюминия и водные растворы гидроксида бария и хлороводорода. Получите из этих веществ семь различных солей (без использования ОВР).
Ответ . Соли: AlCl 3 , BaS, FeCl 2 , BaCl 2 , Ba(OH)Cl, Al(OH)Cl 2 , Al(OH) 2 Cl.
6. При действии концентрированной серной кислоты на бромиды выделяется сернистый газ, а на йодиды – сероводород. Напишите уравнения реакций. Объясните разницу в характере продуктов в этих случаях.
Ответ . Уравнения реакций:
2H 2 SO 4 (конц.) + 2NaBr = SO 2 + Br 2 + Na 2 SO 4 + 2H 2 O,
5H 2 SO 4 (конц.) + 8NaI = H 2 S + 4I 2 + 4Na 2 SO 4 + 4H 2 O.
1 См.: Лидин Р.А. «Справочник по общей и неорганической химии». М.: Просвещение, 1997.
* Знак +/– означает, что данная реакция протекает не со всеми реагентами или в специфических условиях.
Продолжение следует
, , 21 , , ,
, 25-26 , 27-28 , , 30, , , , , , , , , , , , /2003;
, , , , , , , , , , , , , /2004
§ 8.1. Окислительно-восстановительные реакции
ЛАБОРАТОРНЫЕ ИССЛЕДОВАНИЯ
(продолжение)
2. Озон – окислитель.
Озон – важнейшее для природы и человека вещество.
Озон создает вокруг Земли на высоте от 10 до 50 км озоносферу с максимумом содержания озона на высоте 20–25 км. Находясь в верхних слоях атмосферы, озон не пропускает к поверхности Земли большую часть ультрафиолетовых лучей Солнца, губительно действующих на человека, животный и растительный мир. В последние годы обнаружены участки озоносферы с сильно пониженным содержанием озона, так называемые озоновые дыры. Неизвестно, образовывались ли озоновые дыры раньше. Также непонятны и причины их возникновения. Предполагают, что хлорсодержащие фреоны холодильников и парфюмерных баллончиков под действием ультрафиолетового излучения Солнца выделяют атомы хлора, которые реагируют с озоном и тем самым уменьшают его концентрацию в верхних слоях атмосферы. Опасность озоновых дыр в атмосфере крайне беспокоит ученых.
В нижних слоях атмосферы озон образуется в результате ряда последовательных реакций между кислородом воздуха и оксидами азота, выбрасываемыми плохо отрегулированными двигателями автомобилей и создающимися разрядами высоковольтных линий электропередач. Озон очень вреден для дыхания – он разрушает ткани бронхов и легких. Озон чрезвычайно ядовит (сильнее угарного газа). Предельно допустимая концентрация в воздухе – 10 –5 %.
Таким образом, озон в верхних и в нижних слоях атмосферы оказывает противоположное по своим результатам воздействие на человека и животный мир.
Озон наряду с хлором используют для обработки воды, чтобы разрушить органические примеси и уничтожить бактерии. Однако как хлорирование, так и озонирование воды имеет свои преимущества и недостатки. При хлорировании воды уничтожаются практически полностью бактерии, но образуются вредные для здоровья органические вещества канцерогенного характера (способствуют развитию раковых опухолей) – диоксины и подобные им соединения. При озонировании воды такие вещества не образуются, но озон убивает не все бактерии, и оставшиеся живыми бактерии через некоторое время обильно размножаются, поглощая остатки убитых бактерий, и вода становится даже более загрязненной бактериальной флорой. Поэтому озонирование питьевой воды лучше применять при ее быстром использовании. Очень эффективно озонирование воды в бассейнах, когда вода непрерывно циркулирует через озонатор. Озон применяют также и для очистки воздуха. Он относится к числу экологически чистых окислителей, не оставляющих вредных продуктов своего распада.
Озон окисляет почти все металлы, кроме золота и металлов платиновой группы.
Химические способы получения озона неэффективны или слишком опасны. Поэтому советуем вам получить озон в смеси с воздухом в озонаторе (действие слабого электрического разряда на кислород), имеющемся в школьной физической лаборатории.
Озон чаще всего получают действием на газообразный кислород тихого электрического разряда (без свечения и искр), который происходит между стенками внутреннего и внешнего сосудов озонатора. Простейший озонатор нетрудно изготовить из стеклянных трубок с пробками. Как это сделать, вы поймете из рис. 8.4. Внутренний электрод – металлический стержень (длинный гвоздь), наружный электрод – проволочная спираль. Воздух можно продувать воздушным насосом для аквариума или резиновой грушей от пульверизатора. На рис. 8.4 внутренний электрод находится в стеклянной трубке (как вы думаете, почему? ), но можно собрать озонатор и без нее. Резиновые пробки быстро разъедаются озоном.
Высокое напряжение удобно получить от индукционной катушки системы зажигания автомобиля, непрерывно размыкая соединение с источником низкого напряжения (аккумулятор или выпрямитель тока на 12 В).
Выход озона – несколько процентов.
Качественно обнаружить озон можно при помощи
крахмального раствора йодида калия. Этим
раствором можно пропитать полоску
фильтровальной бумаги или раствор добавить в
озонированную воду, а воздух с озоном пропускать
через раствор в пробирке. Кислород в реакцию с
йодид-ионом не вступает.
Уравнение реакции:
2I – + О 3 + Н 2 О = I 2 + O 2 + 2ОН – .
Напишите уравнения реакций приема и отдачи
электронов.
Поднесите к озонатору полоску фильтровальной
бумаги, смоченную этим раствором. (Зачем
раствор йодида калия должен содержать крахмал?)
Определению озона этим способом мешает пероксид
водорода (почему?)
.
Рассчитайте ЭДС реакции, используя электродные
потенциалы:
3. Восстановительные свойства сероводорода и сульфид-иона.
Сероводород – бесцветный газ с запахом тухлых
яиц (в состав некоторых белков входит сера).
Для проведения опытов с сероводородом можно
пользоваться газообразным сероводородом,
пропуская его через раствор с изучаемым
веществом, или приливать к исследуемым растворам
заранее приготовленную сероводородную воду (это
удобнее). Многие реакции можно проводить с
раствором сульфида натрия (реакции на
сульфид-ион S 2–).
Работать с сероводородом только под тягой! Смеси
сероводорода с воздухом сгорают со взрывом.
Сероводород обычно получают в аппарате Киппа, действуя 25%-й серной (разбавленной 1:4) или 20%-й соляной (разбавленной 1:1) кислотой на сульфид железа в виде кусочков размером 1–2 см. Уравнение реакции:
FeS (кр.) + 2Н + = Fe 2+ + H 2 S (г.).
Небольшие количества сероводорода можно получить, поместив кристаллический сульфид натрия в колбу с пробкой, через которую пропущены капельная воронка с краном и отводная трубка. Медленно приливая из воронки 5–10%-ю соляную кислоту (почему не серную?) , колбу постоянно встряхивают покачиванием, чтобы избежать местного скопления непрореагировавшей кислоты. Если этого не делать, неожиданное смешение компонентов может привести к бурной реакции, выталкиванию пробки и разрушению колбы.
Равномерный ток сероводорода получается при нагревании с серой богатых водородом органических соединений, например парафина (1 часть парафина на 1 часть серы, 300 °С).
Для получения сероводородной воды через дистиллированную воду (или прокипяченную) пропускают сероводород. В одном объеме воды растворяется около трех объемов газообразного сероводорода. При стоянии на воздухе сероводородная вода постепенно мутнеет (почему?) .
Сероводород – сильный восстановитель: галогены восстанавливаются им до галогеноводородов, серная кислота – до диоксида серы и серы.
Сероводород ядовит. Предельно допустимая концентрация в воздухе 0,01 мг/л. Даже при незначительных концентрациях сероводород раздражает глаза и дыхательные пути, вызывает головную боль. Концентрации выше 0,5 мг/л опасны для жизни. При более высоких концентрациях поражается нервная система. При вдохе сероводорода возможна остановка сердца и дыхания. Иногда сероводород скапливается в пещерах и канализационных колодцах, и попавший туда человек мгновенно теряет сознание и погибает.
В то же время сероводородные ванны оказывают лечебное действие на организм человека.
3а. Реакция сероводорода с пероксидом водорода.
Изучите действие раствора пероксида водорода
на сероводородную воду или раствор сульфида
натрия.
По результатам опытов составьте уравнения
реакций. Рассчитайте ЭДС реакции и сделайте
вывод о возможности ее прохождения.

3б. Реакция сероводорода с серной кислотой.
В пробирку с 2–3 мл сероводородной воды (или
раствора сульфида натрия) прилейте по каплям
концентрированную серную кислоту (осторожно!)
до появления мути. Что это за вещество? Какие
другие продукты могут получиться в этой реакции?
Напишите уравнения реакций. Рассчитайте ЭДС
реакции, используя электродные потенциалы:

4. Диоксид серы и сульфит-ион.
Диоксид серы, сернистый газ – важнейший загрязнитель атмосферы, выделяемый автомобильными двигателями при использовании плохо очищенного бензина и топками, в которых сгорают серосодержащие угли, торф или мазут. Ежегодно в атмосферу из-за сжигания угля и нефти выбрасываются миллионы тонн диоксида серы.
В природе диоксид серы встречается в вулканических газах. Диоксид серы окисляется кислородом воздуха в триоксид серы, который, поглощая воду (пары), превращается в серную кислоту. Выпадающие кислотные дожди разрушают цементные части построек, памятники архитектуры, высеченные из камня скульптуры. Кислотные дожди замедляют рост растений и даже приводят к их гибели, убивают живые организмы водоемов. Такие дожди вымывают из пашен малорастворимые в воде фосфорные удобрения, которые, попадая в водоемы, приводят к бурному размножению водорослей и быстрому заболачиванию прудов, рек.
Диоксид серы – бесцветный газ с резким запахом. Получать диоксид серы и работать с ним следует под тягой.
Сернистый газ можно получить, поместив в колбу,
закрывающуюся пробкой с отводной трубкой и
капельной воронкой, 5–10 г сульфита натрия. Из
капельной воронки с 10 мл концентрированной
серной кислоты (крайняя осторожность!)
приливайте ее по каплям к кристаллам сульфита
натрия. Вместо кристаллического сульфита натрия
можно воспользоваться его насыщенным раствором.
Диоксид серы можно получить также реакцией между
металлической медью и серной кислотой. В
круглодонную колбу, снабженную пробкой с
газоотводной трубкой и капельной воронкой,
положите медные стружки или куски проволоки и
прилейте из капельной воронки немного серной
кислоты (на 10 г меди берется около 6 мл
концентрированной серной кислоты). Для начала
реакции слегка нагрейте колбу. После этого
кислоту приливайте по каплям. Напишите уравнения
приема и отдачи электронов и суммарное
уравнение.
Свойства диоксида серы можно изучать, пропуская
газ через раствор реагента, или в виде водного
раствора (сернистой кислоты). Такие же результаты
получаются при использовании подкисленных
растворов сульфитов натрия Na 2 SO 3 и
калия К 2 SO 3 . В одном объеме воды
растворяется до сорока объемов сернистого газа
(получается ~6%-й раствор).
Диоксид серы токсичен. При легких отравлениях
начинается кашель, насморк, появляются слезы,
начинается головокружение. Увеличение дозы
приводит к остановке дыхания.
4а. Взаимодействие сернистой кислоты с пероксидом водорода.
Предскажите продукты взаимодействия сернистой
кислоты и пероксида водорода. Проверьте свое
предположение опытом.
К 2–3 мл сернистой кислоты прилейте столько же
3%-го раствора пероксида водорода. Как доказать
образование предполагаемых продуктов реакции?
Тот же опыт повторите с подкисленным и щелочным
растворами сульфита натрия.
Напишите уравнения реакций и рассчитайте ЭДС
процесса.
Выберите нужные вам электродные потенциалы:

4б. Реакция между сернистым газом и сероводородом.
Эта реакция проходит между газообразными SO 2
и H 2 S и служит для получения серы. Реакция
интересна также тем, что два загрязнителя
атмосферы взаимно уничтожают друг друга.
Проходит ли эта реакция между растворами
сероводорода и сернистого газа? Ответьте на этот
вопрос опытом.
Выберите электродные потенциалы для определения
возможности прохождения реакции в растворе:

Попробуйте провести термодинамический расчет возможности прохождения реакций. Термодинамические характеристики веществ для определения возможности прохождения реакции между газообразными веществами следующие:
При каком состоянии веществ – газообразном или в растворе – реакции более предпочтительны?
- (сернистый водород) H2S, бесцветный газ с запахом тухлых яиц; tпл?85,54 .С, tкип?60,35 .С; при 0 .С сжижается под давлением 1 МПа. Восстановитель. Побочный продукт при очистке нефтепродуктов, коксовании угля и др.; образуется при разложении… … Большой Энциклопедический словарь
СЕРОВОДОРОД - (H2S), бесцветный, ядовитый газ с запахом тухлых яиц. Образуется в процессах гниения, содержится в сырой нефти. Получают действием серной кислоты на сульфиды металлов. Используется в традиционном КАЧЕСТВЕННОМ АНАЛИЗЕ. Свойства: температура… … Научно-технический энциклопедический словарь
СЕРОВОДОРОД - СЕРОВОДОРОД, сероводорода, мн. нет, муж. (хим.). Газ, образующийся при гниении белковых веществ, издающий запах тухлых яиц. Толковый словарь Ушакова. Д.Н. Ушаков. 1935 1940 … Толковый словарь Ушакова
СЕРОВОДОРОД - СЕРОВОДОРОД, а, муж. Бесцветный газ с резким неприятным запахом, образующийся при разложении белковых веществ. | прил. сероводородный, ая, ое. Толковый словарь Ожегова. С.И. Ожегов, Н.Ю. Шведова. 1949 1992 … Толковый словарь Ожегова
сероводород - сущ., кол во синонимов: 1 газ (55) Словарь синонимов ASIS. В.Н. Тришин. 2013 … Словарь синонимов
СЕРОВОДОРОД - бесцветный ядовитый газ H2S с неприятным специфическим запахом. Обладает слабокислотными свойствами. 1 л С. при t 0 °C и давлении 760 мм составляет 1,539 г. Встречается в нефтях, в природных водах, в газах биохимического происхождения, как… … Геологическая энциклопедия
СЕРОВОДОРОД - СЕРОВОДОРОД, H2S (молекулярный вес 34,07), бесцветный газ с характерным запахом тухлых яиц. Литр газа при нормальных условиях (0°, 760 мм) весит 1,5392 г. Темп, кипения 62°, плавления 83°; С. входит в состав газообразных выделений… … Большая медицинская энциклопедия
сероводород - — Тематики биотехнологии EN hydrogen sulfide … Справочник технического переводчика
сероводород - СЕРОВОДОРОД, а, м Бесцветный газ с резким неприятным запахом, образующийся при разложении белковых веществ и представляющий собой соединение серы с водородом. Сероводород содержится в некоторых минеральных водах и лечебных грязях и используется… … Толковый словарь русских существительных
Книги
- Как бросить курить! (DVD) , Пелинский Игорь , "Нет ничего легче, чем бросить курить, - я уже тридцать раз бросал" (Марк Твен). Почему люди начинают курить? Чтобы расслабиться, отвлечься, собраться с мыслями, избавиться от стресса или… Категория: Психология. Бизнес Серия: Путь к здоровью и совершенству Издатель: Сова-Фильм , Купить за 275 руб
- Вестиментиферы – бескишечные беспозвоночные морских глубин , В. В. Малахов , Монография посвящена новой группе гигантских (до 2,5 м) глубоководных животных, обитающих в районах глубоководной гидротермальной активности и холодных углеводородных просачиваний. Наиболее… Категория: Медицина Издатель: Товарищество научных изданий КМК , Купить за 176 руб электронная книга (fb2, fb3, epub, mobi, pdf, html, pdb, lit, doc, rtf, txt)
О.С.ЗАЙЦЕВ
УЧЕБНАЯ КНИГА ПО ХИМИИ
ДЛЯ УЧИТЕЛЕЙ СРЕДНИХ ШКОЛ,
СТУДЕНТОВ ПЕДАГОГИЧЕСКИХ ВУЗОВ И ШКОЛЬНИКОВ 9–10
КЛАССОВ,
РЕШИВШИХ ПОСВЯТИТЬ СЕБЯ ХИМИИ И ЕСТЕСТВОЗНАНИЮ
УЧЕБНИКЗАДАЧНИКЛАБОРАТОРНЫЙ ПРАКТИКУМНАУЧНЫЕ РАССКАЗЫ ДЛЯ ЧТЕНИЯ
Продолжение. См. № 4–14, 16–28, 30–34, 37–44, 47,
48/2002;
1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23,
24, 25-26, 27-28, 29, 30, 31, 32, 35, 36, 37, 39, 41, 42, 43, 44 , 46, 47/2003;
1, 2, 3, 4, 5, 7, 11, 13, 14, 16, 17, 20, 22, 24/2004
§ 8.1. Окислительно-восстановительные реакции
ЛАБОРАТОРНЫЕ ИССЛЕДОВАНИЯ
(продолжение)
2. Озон – окислитель.
Озон – важнейшее для природы и человека вещество.
Озон создает вокруг Земли на высоте от 10 до 50 км озоносферу с максимумом содержания озона на высоте 20–25 км. Находясь в верхних слоях атмосферы, озон не пропускает к поверхности Земли большую часть ультрафиолетовых лучей Солнца, губительно действующих на человека, животный и растительный мир. В последние годы обнаружены участки озоносферы с сильно пониженным содержанием озона, так называемые озоновые дыры. Неизвестно, образовывались ли озоновые дыры раньше. Также непонятны и причины их возникновения. Предполагают, что хлорсодержащие фреоны холодильников и парфюмерных баллончиков под действием ультрафиолетового излучения Солнца выделяют атомы хлора, которые реагируют с озоном и тем самым уменьшают его концентрацию в верхних слоях атмосферы. Опасность озоновых дыр в атмосфере крайне беспокоит ученых.
В нижних слоях атмосферы озон образуется в результате ряда последовательных реакций между кислородом воздуха и оксидами азота, выбрасываемыми плохо отрегулированными двигателями автомобилей и создающимися разрядами высоковольтных линий электропередач. Озон очень вреден для дыхания – он разрушает ткани бронхов и легких. Озон чрезвычайно ядовит (сильнее угарного газа). Предельно допустимая концентрация в воздухе – 10 –5 %.
Таким образом, озон в верхних и в нижних слоях атмосферы оказывает противоположное по своим результатам воздействие на человека и животный мир.
Озон наряду с хлором используют для обработки воды, чтобы разрушить органические примеси и уничтожить бактерии. Однако как хлорирование, так и озонирование воды имеет свои преимущества и недостатки. При хлорировании воды уничтожаются практически полностью бактерии, но образуются вредные для здоровья органические вещества канцерогенного характера (способствуют развитию раковых опухолей) – диоксины и подобные им соединения. При озонировании воды такие вещества не образуются, но озон убивает не все бактерии, и оставшиеся живыми бактерии через некоторое время обильно размножаются, поглощая остатки убитых бактерий, и вода становится даже более загрязненной бактериальной флорой. Поэтому озонирование питьевой воды лучше применять при ее быстром использовании. Очень эффективно озонирование воды в бассейнах, когда вода непрерывно циркулирует через озонатор. Озон применяют также и для очистки воздуха. Он относится к числу экологически чистых окислителей, не оставляющих вредных продуктов своего распада.
Озон окисляет почти все металлы, кроме золота и металлов платиновой группы.
Химические способы получения озона неэффективны или слишком опасны. Поэтому советуем вам получить озон в смеси с воздухом в озонаторе (действие слабого электрического разряда на кислород), имеющемся в школьной физической лаборатории.
Озон чаще всего получают действием на газообразный кислород тихого электрического разряда (без свечения и искр), который происходит между стенками внутреннего и внешнего сосудов озонатора. Простейший озонатор нетрудно изготовить из стеклянных трубок с пробками. Как это сделать, вы поймете из рис. 8.4. Внутренний электрод – металлический стержень (длинный гвоздь), наружный электрод – проволочная спираль. Воздух можно продувать воздушным насосом для аквариума или резиновой грушей от пульверизатора. На рис. 8.4 внутренний электрод находится в стеклянной трубке (как вы думаете, почему? ), но можно собрать озонатор и без нее. Резиновые пробки быстро разъедаются озоном.
 |
Высокое напряжение удобно получить от индукционной катушки системы зажигания автомобиля, непрерывно размыкая соединение с источником низкого напряжения (аккумулятор или выпрямитель тока на 12 В).
Выход озона – несколько процентов.
Качественно обнаружить озон можно при помощи
крахмального раствора йодида калия. Этим
раствором можно пропитать полоску
фильтровальной бумаги или раствор добавить в
озонированную воду, а воздух с озоном пропускать
через раствор в пробирке. Кислород в реакцию с
йодид-ионом не вступает.
Уравнение реакции:
2I – + О 3 + Н 2 О = I 2 + O 2 + 2ОН – .
Напишите уравнения реакций приема и отдачи
электронов.
Поднесите к озонатору полоску фильтровальной
бумаги, смоченную этим раствором. (Зачем
раствор йодида калия должен содержать крахмал?)
Определению озона этим способом мешает пероксид
водорода (почему?)
.
Рассчитайте ЭДС реакции, используя электродные
потенциалы:
3. Восстановительные свойства сероводорода и сульфид-иона.
Сероводород – бесцветный газ с запахом тухлых
яиц (в состав некоторых белков входит сера).
Для проведения опытов с сероводородом можно
пользоваться газообразным сероводородом,
пропуская его через раствор с изучаемым
веществом, или приливать к исследуемым растворам
заранее приготовленную сероводородную воду (это
удобнее). Многие реакции можно проводить с
раствором сульфида натрия (реакции на
сульфид-ион S 2–).
Работать с сероводородом только под тягой! Смеси
сероводорода с воздухом сгорают со взрывом.
Сероводород обычно получают в аппарате Киппа, действуя 25%-й серной (разбавленной 1:4) или 20%-й соляной (разбавленной 1:1) кислотой на сульфид железа в виде кусочков размером 1–2 см. Уравнение реакции:
FeS (кр.) + 2Н + = Fe 2+ + H 2 S (г.).
Небольшие количества сероводорода можно получить, поместив кристаллический сульфид натрия в колбу с пробкой, через которую пропущены капельная воронка с краном и отводная трубка. Медленно приливая из воронки 5–10%-ю соляную кислоту (почему не серную?) , колбу постоянно встряхивают покачиванием, чтобы избежать местного скопления непрореагировавшей кислоты. Если этого не делать, неожиданное смешение компонентов может привести к бурной реакции, выталкиванию пробки и разрушению колбы.
Равномерный ток сероводорода получается при нагревании с серой богатых водородом органических соединений, например парафина (1 часть парафина на 1 часть серы, 300 °С).
Для получения сероводородной воды через дистиллированную воду (или прокипяченную) пропускают сероводород. В одном объеме воды растворяется около трех объемов газообразного сероводорода. При стоянии на воздухе сероводородная вода постепенно мутнеет (почему?) .
Сероводород – сильный восстановитель: галогены восстанавливаются им до галогеноводородов, серная кислота – до диоксида серы и серы.
Сероводород ядовит. Предельно допустимая концентрация в воздухе 0,01 мг/л. Даже при незначительных концентрациях сероводород раздражает глаза и дыхательные пути, вызывает головную боль. Концентрации выше 0,5 мг/л опасны для жизни. При более высоких концентрациях поражается нервная система. При вдохе сероводорода возможна остановка сердца и дыхания. Иногда сероводород скапливается в пещерах и канализационных колодцах, и попавший туда человек мгновенно теряет сознание и погибает.
В то же время сероводородные ванны оказывают лечебное действие на организм человека.
3а. Реакция сероводорода с пероксидом водорода.
Изучите действие раствора пероксида водорода
на сероводородную воду или раствор сульфида
натрия.
По результатам опытов составьте уравнения
реакций. Рассчитайте ЭДС реакции и сделайте
вывод о возможности ее прохождения.

3б. Реакция сероводорода с серной кислотой.
В пробирку с 2–3 мл сероводородной воды (или
раствора сульфида натрия) прилейте по каплям
концентрированную серную кислоту (осторожно!)
до появления мути. Что это за вещество? Какие
другие продукты могут получиться в этой реакции?
Напишите уравнения реакций. Рассчитайте ЭДС
реакции, используя электродные потенциалы:

4. Диоксид серы и сульфит-ион.
Диоксид серы, сернистый газ – важнейший загрязнитель атмосферы, выделяемый автомобильными двигателями при использовании плохо очищенного бензина и топками, в которых сгорают серосодержащие угли, торф или мазут. Ежегодно в атмосферу из-за сжигания угля и нефти выбрасываются миллионы тонн диоксида серы.
В природе диоксид серы встречается в вулканических газах. Диоксид серы окисляется кислородом воздуха в триоксид серы, который, поглощая воду (пары), превращается в серную кислоту. Выпадающие кислотные дожди разрушают цементные части построек, памятники архитектуры, высеченные из камня скульптуры. Кислотные дожди замедляют рост растений и даже приводят к их гибели, убивают живые организмы водоемов. Такие дожди вымывают из пашен малорастворимые в воде фосфорные удобрения, которые, попадая в водоемы, приводят к бурному размножению водорослей и быстрому заболачиванию прудов, рек.
Диоксид серы – бесцветный газ с резким запахом. Получать диоксид серы и работать с ним следует под тягой.
Сернистый газ можно получить, поместив в колбу,
закрывающуюся пробкой с отводной трубкой и
капельной воронкой, 5–10 г сульфита натрия. Из
капельной воронки с 10 мл концентрированной
серной кислоты (крайняя осторожность!)
приливайте ее по каплям к кристаллам сульфита
натрия. Вместо кристаллического сульфита натрия
можно воспользоваться его насыщенным раствором.
Диоксид серы можно получить также реакцией между
металлической медью и серной кислотой. В
круглодонную колбу, снабженную пробкой с
газоотводной трубкой и капельной воронкой,
положите медные стружки или куски проволоки и
прилейте из капельной воронки немного серной
кислоты (на 10 г меди берется около 6 мл
концентрированной серной кислоты). Для начала
реакции слегка нагрейте колбу. После этого
кислоту приливайте по каплям. Напишите уравнения
приема и отдачи электронов и суммарное
уравнение.
Свойства диоксида серы можно изучать, пропуская
газ через раствор реагента, или в виде водного
раствора (сернистой кислоты). Такие же результаты
получаются при использовании подкисленных
растворов сульфитов натрия Na 2 SO 3 и
калия К 2 SO 3 . В одном объеме воды
растворяется до сорока объемов сернистого газа
(получается ~6%-й раствор).
Диоксид серы токсичен. При легких отравлениях
начинается кашель, насморк, появляются слезы,
начинается головокружение. Увеличение дозы
приводит к остановке дыхания.
4а. Взаимодействие сернистой кислоты с пероксидом водорода.
Предскажите продукты взаимодействия сернистой
кислоты и пероксида водорода. Проверьте свое
предположение опытом.
К 2–3 мл сернистой кислоты прилейте столько же
3%-го раствора пероксида водорода. Как доказать
образование предполагаемых продуктов реакции?
Тот же опыт повторите с подкисленным и щелочным
растворами сульфита натрия.
Напишите уравнения реакций и рассчитайте ЭДС
процесса.
Выберите нужные вам электродные потенциалы:

4б. Реакция между сернистым газом и сероводородом.
Эта реакция проходит между газообразными SO 2
и H 2 S и служит для получения серы. Реакция
интересна также тем, что два загрязнителя
атмосферы взаимно уничтожают друг друга.
Проходит ли эта реакция между растворами
сероводорода и сернистого газа? Ответьте на этот
вопрос опытом.
Выберите электродные потенциалы для определения
возможности прохождения реакции в растворе:

Попробуйте провести термодинамический расчет возможности прохождения реакций. Термодинамические характеристики веществ для определения возможности прохождения реакции между газообразными веществами следующие:
При каком состоянии веществ – газообразном или в растворе – реакции более предпочтительны?
Серная кислота – один из основных много тоннажных продуктов химической промышленности. Ее применяют в различных отраслях народного хозяйства, поскольку она обладает комплексом особых свойств, облегчающих ее технологическое использование. Серная кислота не дымит, не имеет цвета, запаха, при обычной температуре находится в жидком состоянии. В концентрированном виде не корродирует черные металлы. В то же время серная кислота относится к числу сильных минеральных кислот, образует многочисленные устойчивые соли и дешева. Безводная серная кислота (моногидрат) Н2SО4 представляет собой тяжелую маслянистую жидкость, которая смешивается с водой во всех соотношениях с выделением большого количества тепла.
Сырье процесса: серный колчедан, элементная сера, сероводород, сульфиды металлов, такие как медный колчедан CuFeS 2 , медный блеск CuS 2 , сульфаты : гипс CaSO 4 2H 2 O, ангидрит CaSO 4 , мирабилит Na 2 SO 4 10H 2 O и т.д.
Получение газовой серы из сероводорода, извлекаемого при очистке горючих и технологических газов, основано на процессе неполного окисления на твердом катализаторе. При этом протекают реакции:
H 2 S + 1,5O 2 = SO 2 + H 2 O;
2H 2 S + SO 2 = 2H 2 O + 1,5S 2 .
Значительные количества серы могут быть получены из побочных продуктов производства цветных металлов, например меди:
2FeS 2 = 2FeS +S 2 ;
SO 2 + C = S + CO 2 ;
CS 2 + SO 2 = 1,5S 2 + CO 2 ;
2COS + SO 2 = 1,5S 2 + 2CO 2
Получение сернистого газа сжиганием серы, сероводорода и других видов сырья
При сжигании 1 моля серы расходуется 1 моль кислорода. При этом получают 1 моль сернистого газа:
S (газ) + О2 (газ) = S02 (газ)-j - 362,4 кДж (86,5 ккал).
Поэтому при горении серы в воздухе, содержащем 21% кислорода, возможно (теоретически) получить 21% сернистого ангидрида. Выход сернистого ангидрида здесь выше, чем при горении колчедана и цинковой обманки. При сжигании серы в производстве серной кислоты получается наиболее выгодное соотношение SO2 и кислорода. Если сжигать серу с небольшим избытком воздуха, можно получить сернистый газ с повышенным содержанием S02. Однако при этом развивается темпе ратура до 1300°С, что приводит к разрушению футеровки печи; это ограничивает получение из серы газа с высокой концентрацией S02.
Сероводород сгорает с образованием S02 и Н20:
2H2S + 302 = 2S02+2H20-f 1038,7 кДж (247,9 ккал).
Образующиеся при этом пары воды поступают с газовой смесью в контактный аппарат, а из него на абсорбцию.
По технологическому оформлению производство серной кислоты из железного колчедана является наиболее сложным процессом и состоит из нескольких последовательно проводимых стадий.
Принципиальная схема этого производства представлена на рисунке.
1 – получение обжигового газа: 1 – обжиг колчедана, 2 – охлаждение газа в котле-утилизаторе, 3 – общая очистка газа, 4 – специальная очистка газа; 11 – контактирование: 5 – подогрев газа в теплообменнике, 6 – контактирование; 111 – абсорбция: 7 – абсорбция оксида серы (6) и образование серной кислоты.

Сернистый ангидрид S02 – это бесцветный газ, в 2.3 раза тяжелее воздуха, с резким запахом. При растворении в воде образуется слабая и нестойкая сернистая кислота SO2 +Н2О = H2SO3.
2.Уголь. Получение кокса.
Коксование каменных углей
Значительную часть углей подвергают высокотемпературной (пирогене-тической) химической переработке. Цель такой переработки – производство ценных вторичных продуктов, используемых далее в качестве топлива и промежуточных продуктов для органического синтеза. По назначению и условиям процессы пирогенетической переработки углей делят на три вида: пиролиз, газификация, гидрирование .
Пиролиз или сухая перегонка – это процесс нагрева твердого топлива без доступа воздуха с целью получения газообразных, жидких и твердых продуктов различного назначения. Существует высокотемпературный пиролиз (коксование ) и низкотемпературный пиролиз (полукоксование ).
Полукоксование проводят при 500–580 о С с целью получения искусственного жидкого и газообразного топлива. Продуктами полукоксования являются сырье для оргсинтеза, смола (источник получения моторных топлив), растворители, мономеры и полукокс, используемый как местное топливо и добавка в шихту для коксования.
Процессы гидрирования и газификации используются для получения из угля жидких продуктов, применяемых как моторное топливо, и горючих газов.
Коксование каменного угля проводят при температуре 900 – 1200 о С с целью получения кокса, горючих газов и сырья для химической промышленности.
Предприятия, на которых осуществляют коксование углей, называют коксохимическими. Существуют отдельные коксохимические заводы с полным циклом коксохимического производства, размещаемые отдельно от ме-таллургических предприятий, и коксохимические цеха в составе металлургических комбинатов.
Структурная схема коксохимического производства представлена на рисунке.
Каменный уголь
Углеподготовка
Угольная шихта
Кокс
Коксование
ВодородОКГ
ПКГ Кокс на склад
Охлаждение и разделение
СБ КУС
Разгонка
Разгонка
Индивидуальные арены Фракции КУС
Нейтрализация
на переработку
Серная кислота
Сульфат аммония
Рис.. Структурная схема коксохимического производства
На схеме обозначено: ОКГ – обратный коксовый газ; ПКГ – прямой коксовый газ; КУС – каменноугольная смола; СБ – сырой бензол.
По физико-химической природе коксование – это сложный двухфазный эндотермический процесс, в котором протекают термофизические превращения коксуемого сырья и вторичные реакции с участием органических полупродуктов первой стадии коксования. Коксование угля ведут в коксовых печах периодического действия, в которых теплота передается к коксуемой угольной шихте через стенку реактора.
3. Получение соляной кислоты. Соля́ная кислота́ (хлороводоро́дная, хлористоводоро́дная, хлористый водород) - HCl, раствор хлороводорода в воде; сильная одноосновная кислота. Бесцветная (техническая соляная кислота желтоватая из-за примесей Fe, Cl 2 и др.), «дымящая» на воздухе, едкая жидкость. Максимальная концентрация при 20 °C равна 38% по массе, плотность такого раствора 1,19 г/см³. Молярная масса 36,46 г/моль. Соли соляной кислоты называются хлоридами. Рассмотрим основные направления использования кислоты:
Металлургия. Соляная кислота техническая применяется для зачистки металлов при лужении и паянии. Также кислота соляная используется при получении марганца, железа и других веществ.
Гальванопластика. В этом направлении соляная кислота техническая выступает в роли активной среды при травлении и декапировании.
Пищевая промышленность. Всевозможные регуляторы кислотности, например, E507, имеют в своем составе кислоту. Да и содовую (сельтерскую) воду трудно представить без такого вещества, как кислота соляная .
Медицина. В данной сфере, конечно же, используется не соляная кислота техническая , а очищенные аналоги, однако, подобное явление все же имеет место. В частности, речь идет о добавлении вещества в желудочный сок в случае недостаточной кислотности.

В колонне адиабатической абсорбции получают соляную кислоту пониженной концентрации, но свободную от органических примесей. Кислоту с повышенной концентрацией HCI производят в колонне изотермической абсорбции при пониженной температуре. Степень извлечения HCI из абгазов при использовании в качестве абсорбентов разбавленных кислот составляет 90-95%. При использовании в качестве абсорбента чистой воды степень извлечения почти полная.
4. Прямой синтез концентрированной азотной кислоты.
Прямой синтез HNО 3 основан на взаимодействии жидких оксидов азота с водой и газообразным кислородом под давлением до 5 МПа по уравнению
2N 2 O 4 + O 2 + 2H 2 O → 4HNO 3
100%-ный диоксид азота при атмосферном давлении и температуре 21,5 °С полностью переходит в жидкое состояние. При окислении аммиака полученный NO окисляется в NO 2 , содержание которого в газовой смеси составляет около 11%. Перевести диоксид азота такой концентрации в жидкое состояние при атмосферном давлении не представляется возможным, поэтому для сжижения оксидов азота применяют повышенное давление.
Концентрирование азотной кислоты с помощью водоотнимающих веществ. Получить концентрированную азотную кислоту перегонкой разбавленной кислоты невозможно. При кипении и перегонке разбавленной азотной кислоты ее можно упарить лишь до содержания 68,4 % HNO 3 (азеотропная смесь), после чего состав перегоняемой смеси не изменится.
В промышленности перегонку разбавленных водных растворов азотной кислоты осуществляют в присутствии водоотнимающих веществ (концентрированная серная кислота, фосфорная кислота, концентрированные растворы нитратов и др.). Применение водоотнимающих веществ дает возможность понизить содержание водяных паров над кипящей смесью и увеличить содержание паров азотной кислоты, при конденсации которых получается 98%-ная HNО 3 .
Технологическая схема концентрирования азотной кислоты с применением серной кислоты:

Рисунок– Схема концентрирования разбавленной азотной кислоты в присутствии серной кислоты:
1, 4 – напорные баки для азотной и серной кислоты; 2 – контрольные фонари; 3 – испаритель разбавленной азотной кислоты; 5 – коробка для регулировании подачи кислоты,;6 – концентрационная колонна, 7 – холодильник конденсатор; 8 – холодильник кислоты, циркулирующей в башне; 9 –вентилятор: 10 – поглотительная башня; 11 – сборник; 12 – насос; 13 – холодильник концентрированной азотной кислоты, 14 – холодильник отработанной серной кислоты
Разбавленная азотная кислота из напорного бака 1 подается в колонну 6 через два расходомера 2, включенные параллельно. Один поток кислоты проходит в испаритель 3 и подается в виде смеси жидкости и пара на 10-ю тарелку колонны 6, другой поток без подогрева поступает на вышележащую тарелку.
Серная кислота из напорного бака 4 через регулятор 5 подается в верхнюю часть колонны 6 выше ввода холодного потока азотной кислоты. В нижнюю часть колонны вводится острый пар, при нагревании которым из тройной смеси начинает испаряться азотная кислота.
Пары азотной кислоты при температуре 70–85 °С, поднимаясь вверх, выходят через штуцер в крышке колонны и поступают в холодильник-конденсатор 7. В этих парах имеются примеси оксидов азота и воды.
В холодильнике-конденсаторе пары азотной кислоты при температуре около 30 °С конденсируются с образованием 98–99%-ной HNО 3 , при этом оксиды азота частично поглощаются этой кислотой. Концентрированная азотная кислота, содержащая оксиды азота, направляется на две верхние тарелки и проходит их последовательно, причем оксиды выдуваются из раствора парами азотной кислоты, поступающими в конденсатор 7. Несконденсировавшиеся пары азотной кислоты и выделившиеся оксиды азота направляют на абсорбцию в башню 10, орошаемую водой. Полученная 50%-ная кислота поступает в сборник 11 и вновь направляется на концентрирование. Концентрированную азотную кислоту после охлаждения направляют на склад готовой продукции.
Отработанная серная кислота, содержащая 65–85% H 2 SO 4 , поступает на концентрирование. При концентрировании азотной кислоты с применением 92–93%-ной серной кислоты расход последней значительно сокращается при подаче на концентрирование 59–60%-ной HNO 3 вместо 48–50%-ной. Поэтому в некоторых случаях выгодно проводить предварительное концентрирование 50%-ной HNO 3 до 60%-ной путем простого упаривания.
Большим недостатком концентрирования азотной кислоты с помощью серной кислоты является высокое содержание паров и тумана H 2 SO 4 в выхлопных газах после электрофильтров (0,3–0,8 г/м 3 газа). Поэтому серную кислоту заменяют, например, нитратом магния или цинка.
5. Получение керамики.
Кера́мика - обширная по составу группа диэлектрических материалов, объединенных общностью технологического цикла. В настоящее время под словом керамика понимают не только глиносодержащие, но и другие неорганические материалы, обладающие сходными свойствами, при изготовлении изделий из которых требуется высокотемпературный обжиг. Исходные материалы. Для изготовления керамических изделий используют различные природные и искусственные материалы.
Искусственные и природные материалы - оксиды, соли различаются по количественному и качественному содержанию примесей посторонних оксидов и в соответствии с этим условно обозначают буквами: Ч (чистый), ЧДА (чистый для анализа), ХЧ (химически чистый), и др. Также различают исходное сырье по физико-химическим показателям (размерам и форме частиц, удельной поверхности, активности и др.).
Исходным сырьем для производства радио- и пьезокерамики является большое количество различных солей и окислов: каолины, глины, полевые шпаты, кремний содержащие материалы, тальки - природные пластичные материалы; искусственные непластичные материалы, производимые промышленностью - технический глинозем и корунд, диоксиды циркония и титана, оксид бериллия, карбонаты бария и стронция.
Глины и каолины состоят преимущественно из гидроалюмосиликатов (Al 2 O 3 *2SiO 2 *H 2 O) и примесей солей железа, щелочных и щелочноземельных оксидов и солей. Из полевых шпатов наиболее приемлемы для производства керамики калиево-натриевые полевые шпаты (K 2 O*Al 2 O 3 *6SiO 2 ; Na 2 O*Al 2 O 3 *6SiО 2). Основой кремний содержащих материалов и кварцев является диоксид кремния (SiO 2), в котором могут быть различные добавки (окислы железа, глины, полевые шпаты и др.).Состав тальков разнообразен: от 3MgO*4SiO 2 *H2O до 4MgO*5SiO 2 *H2O, примеси в них Fe 2 O 3 , Al 2 O 3 , CaO, Na 2 О, Cr 2 O и др. Самыми нежелательными примесями во всех природных пластичных материалах являются соли железа.
Названные природные пластичные материалы используют для улучшения пластических свойств пресс-масс для формования изделий и как стеклообразуюшие добавки в радиокерамике. Тальки являются основой таких видов радиокерамики как стеатитовая и форстеритовая.
Технический глинозем и корунд получают при химической переработке природного сырья-минерала боксита и прокаливания его до 1100–1200 0 С. Диоксиды циркония (Zr 2 O 2), титана (TiO 2), олова (SnO 2), оксиды бериллия (B 2 O), стронция (SrO), цинка (ZnO), свинца (PbO), магния (MgO) получают при воздействии на исходное сырье путем комплекса химических и термических взаимодействий.
Получение керамики. По строению керамика представляет собой сложную систему состоящую из трех основных фаз: кристаллической, стекловидной и газовой. Кристаллическая фаза (основная) представляет собой химические соединения или твердые растворы, она определяет характерные свойства керамического материала; стекловидная фаза находится в керамическом материале в виде прослоек между кристаллической составляющей или обособленных микрочастиц и выполняет роль связующего вещества; газовая фаза представляет собой газы, содержащиеся в порах керамики. Поры ухудшают свойства керамики, особенно при повышенной влажности.
Свойства керамики зависят от состава смеси (химического и процентного соотношения веществ), режима обработки.
Керамика может быть изготовлена путем однократного или двукратного обжига. Это имеет свои преимущества и недостатки.
В производстве керамики распространены следующие технологические способы изготовления пъезокерамики основанные на:
1) механическом смешивании исходных веществ в виде порошков окислов и солей металлов, соответствующих химическому составу изготовляемого материала;
2) термическом разложении солей металлов;
3) совместном осаждении карбонатов солей соответствующих металлов или их гидратов.
Исходными веществами для изготовления радио - пъезокерамики и ферритов являются окислы и соли металлов. Основные этапы технологического процесса заключаются в следующем.
Набор исходных веществ определяется заданными магнитными и электрическими свойствами изделий, геометрической формой и размерами.
Анализ исходных окислов и солей выполняется с целью определения их физико-химических характеристик, вида и количества примесей, величины и формы частичек, активности, т.е. возможности вступать в реакцию с другими компонентами смеси, и др.
Расчет массы и соотношения исходных компонентов проводят, основываясь на химической формуле материала. И затем в соответствии с расчетом производят взвешивание исходных компонентов.
Помол или растворение и смешивание выполняют для получения однородной по химическому составу и размеру частиц смеси. Эти операции выполняют или с жидкостью (водой) или без воды, т.е. выполняют мокрый (шликерный) или сухой помол. Мокрый помол завершается сушкой.
Операция брикетирование (гранулирование) нужна для получения более компактной формы полученной смеси (шихты) и более полного протекания реакции при выполнении следующей операции. Здесь получают брикеты, таблетки или гранулы.
Предварительный обжиг шихты выполняется для частичного или полного протекания диффузионных процессов между окислами для превращения их в керамический материал (синтез керамики) и уменьшения усадки при окончательном обжиге.
Вторичный помол и смешивание брикетов, таблеток или гранул выполняется с целью получения изделий с равномерными свойствами, полного протекания диффузионных процессов и обеспечивая возможности формирования изделия. Операция выполняется в воде или без воды, а поэтому после ее завершения, как и в первом случае, полученную смесь сушат.
Для улучшения формования порошков в них вводят пластификаторы (связки, смазки), улучшающие адгезию отдельных частиц. Введение пластификаторов дает возможность получать различные массы: для прессования – пресс - порошки, для литья - шликеры, а для формирования из пластичных масс - пластичные массы.
Основными способами формирования являются прессование, формование из пластичных масс, шликерное литье.
Отформованные изделия подвергают высокотемпературному спеканию, при котором получают соответствующий данному материалу (радио-, пьезокерамике, ферриту) комплекс определенных магнитных, электрических, механических свойств и физико-механических характеристик.
6. Получение гидроксида натрия. Гидроксид натрия может получаться в промышленности химическими и электрохимическими методами.